取碳酸钠和氯化钠的白色固体混合物l4.6g 与68.3g一定质量分数的稀盐酸混合 恰好完全反应 所得
| 取碳酸钠和氯化钠的白色固体混合物l4.6g,与68.3g一定质量分数的稀盐酸混合,恰好完全反应,所得溶液的质量为78.5g。试计算: (1)生成气体的质量; (2)反应后所得溶液中溶质的质量分数。 |
参考解答
| 解:(1)气体的质量=14.6g+68.3g-78.5g=4.4g (2)设混合物中Na2CO3的质量为x,生成NaCl的质量为y。 Na2CO3+2HCl==2NaCl+H2O+CO2↑ 106 117 44 x y 4.4g  10.6g 10.6g 11.7g 11.7gNaCl的总质量=(l4.6g-10.6g)+11.7g=15.7g 反应后溶液中溶质质量分数为: 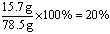 答:生成气体的质量为4.4g,反应后所得溶液中溶质质量分数为20%。 |
相似问题
CaCO3在高温条件下分解生成CaO和CO2 计算高温分解200gCaCO3生成CaO的质量。
CaCO3在高温条件下分解生成CaO和CO2,计算高温分解200gCaCO3生成CaO的质量。
某同学在参加学校开展的综合实践活动中 考察了一家化工厂的污水处理情况。该同学考察过程中收集到以下资料
某同学在参加学校开展的综合实践活动中,考察了一家化工厂的污水处理情况。该同学考察过程中收集到以下资料:(1)该化工厂排放的污水中主要成分是盐酸,提
现有4gCu和另一种金属的混合物 将其加入足量的稀盐酸充分反应后得到0.2g氢气 则另一种金属是[
现有4gCu和另一种金属的混合物,将其加入足量的稀盐酸充分反应后得到0 2g氢气,则另一种金属是[ ]A AB BC CD D
天然气的主要成分是甲烷(CH4) 其燃烧会产生二氧化碳和水 反应过程为:CH4+2O2CO2+2H2
天然气的主要成分是甲烷(CH4),其燃烧会产生二氧化碳和水,反应过程为:CH4+2O2CO2+2H2O,请计算:(1)甲烷的相对分子质量________________,(2)甲
某同学对某地工业废水(含有硫酸和盐酸)中的H2SO4进行测定。取50g该废水于烧杯中 加入足量的Ba
某同学对某地工业废水(含有硫酸和盐酸)中的H2SO4进行测定。取50g该废水于烧杯中,加入足量的BaCl2溶液,充分反应中,过滤、洗涤、干燥得到BaSO4固体11












