某同学对某地工业废水(含有硫酸和盐酸)中的H2SO4进行测定。取50g该废水于烧杯中 加入足量的Ba
| 某同学对某地工业废水(含有硫酸和盐酸)中的H2SO4进行测定。取50g该废水于烧杯中,加入足量的BaCl2溶液,充分反应中,过滤、洗涤、干燥得到BaSO4固体11.65g。通过计算回答下列问题: (1)50g该废水中H2SO4的质量。 (2)若改用KOH溶液来测定50g该废水中H2SO4的含量,结果会_________(填“偏高”、“偏低”、“不变”),理由是____________________。 |
参考解答
| 解:(1)设硫酸的质量为X。 H2SO4+BaCl2==BaSO4  +2HCl +2HCl98 233 X 11.65g 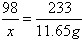 ;X=4.9g ;X=4.9g答:硫酸的质量为4.9g (2)偏高;说到盐酸跟氢氧化钾反应即可。 |
相似问题
某化学兴趣小组为了测定一批石灰石样品中碳酸钙的质量分数 取用4 g石灰石样品 将40g稀盐酸分为4次
某化学兴趣小组为了测定一批石灰石样品中碳酸钙的质量分数,取用4 g石灰石样品,将40g稀盐酸分为4次加入样品中(石灰石样品中所含的杂质不溶于水和盐酸)
某同学称取10. 6g的不纯的纯碱粉末样品[含杂质可能是①NaHCO3②K2CO3③NaCl]跟足量
某同学称取10 6g的不纯的纯碱粉末样品[含杂质可能是①NaHCO3②K2CO3③NaCl]跟足量的稀盐酸反应,共收集到4 5g的CO2,则样品中 [ ]A.肯定含有①②③B.肯
十堰市是南水北调工程的水源地之一。近日市环保局对某工厂含少量硫酸的废水进行了抽样检查:取一定量废水用
十堰市是南水北调工程的水源地之一。近日市环保局对某工厂含少量硫酸的废水进行了抽样检查:取一定量废水用1%的氢氧化钠溶液中和(其它杂质不与氢氧化钠反
如图所示 在托盘天平两边各放一只相同质量的烧杯 向两只烧杯里注入溶质质量分数相同 质量相等的足量稀盐
如图所示,在托盘天平两边各放一只相同质量的烧杯,向两只烧杯里注入溶质质量分数相同、质量相等的足量稀盐酸,进行如下实验: 第一步:向左盘烧杯里投
某课外活动小组利用稀硫酸测定粗锌中纯锌的含量。现称取粗锌20g 加入到足量硫酸溶液中充分反应(杂质不
某课外活动小组利用稀硫酸测定粗锌中纯锌的含量。现称取粗锌20g,加入到足量硫酸溶液中充分反应(杂质不参与反应),测得数据如下表:(1)计算反应过程












