某实验小组利用如下仪器组装一套制备氮化硼晶体的装置.反应原理是B2O3+2NH3 高温 . 2BN
某实验小组利用如下仪器组装一套制备氮化硼晶体的装置.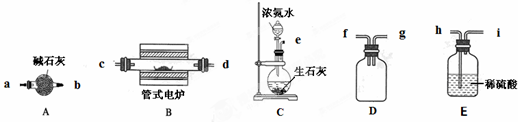 反应原理是B2O3+2NH3
(1)各仪器接口由左到右的连接顺序为______. (2)装置C能产生氨气的原因有______(答出其中一项即可). (3)管式电炉加热反应前必须进行的一步操作是______. |
参考解答
| (1)根据题给信息,干燥氨气和氧化硼反应可制得氮化硼,C为制取氨气的装置,A为干燥装置,B为氮化硼的制取装置,D为安全瓶防倒吸,E为尾气吸收装置,由装置用途可知连接顺序为:e-→a→b→c→d→f→g→h; 故答案为:e-→a→b→c→d→f→g→h; (2)氨水中存在如下平衡:NH3+H2O?NH3?H2O?NH4++OH-,生石灰与水反应生成氢氧化钙并放热,增大了氢氧根浓度, 减少了水的量,平衡逆向移动,生成氨气,同时放热使一水合氨分解,减少了氨气的溶解度,故增大了氨气逸出速率. 故答案为:生石灰与水反应消耗水,促使氨气放出;或生石灰与水反应生成氢氧化钙电离出大量OH-,反应逆向进行有利于NH3放出;或生石灰与水反应放出大量热,促进NH3?H2O分解,并使气体溶解度下降,有利于NH3放出. (3)因氮化硼高温下能被氧化,故管式电炉加热反应前必须进行的一步操作是除去装置中的氧气, 故答案为:除去装置中的氧气. |
相似问题
某同学想通过下图装置(夹持装置已略去)实验 探究SO2与Na2O2反应的产物.Ⅰ.装置D的作用___
某同学想通过下图装置(夹持装置已略去)实验,探究SO2与Na2O2反应的产物.Ⅰ.装置D的作用______.Ⅱ.如何检验反应中是否有O2生成______.Ⅲ.对C中固
下列各组物质的水溶液不用其它试剂无法鉴别的是( )A.NaOH AlCl3B.CuSO4BaCl2
下列各组物质的水溶液不用其它试剂无法鉴别的是( )A.NaOHAlCl3B.CuSO4BaCl2C.NaAlO2HClD.MgCl2NaCl
金属钠与水的反应是中学化学中的一个重要反应.在高中化学教材的几次改版中该实验曾出现过几种不同的演示方
金属钠与水的反应是中学化学中的一个重要反应.在高中化学教材的几次改版中该实验曾出现过几种不同的演示方法,分别如图中甲、乙、丙所示:(1)现按图甲
Cu+在酸性溶液中不稳定 可发生自身氧化-还原反应生成Cu2+和Cu.现有浓硫酸 浓硝酸 稀硫酸 稀
Cu+在酸性溶液中不稳定,可发生自身氧化-还原反应生成Cu2+和Cu.现有浓硫酸、浓硝酸、稀硫酸、稀硝酸、FeCl3稀溶液及pH试纸,而没有其它试剂.简述如何用
能把K2SO4 Ba(NO3)2 Na2CO3三种无色溶液鉴别出来的一种试剂是( )A.KNO3溶
能把K2SO4、Ba(NO3)2、Na2CO3三种无色溶液鉴别出来的一种试剂是( )A.KNO3溶液B.稀硫酸C.NaOH溶液D.Na2SO4溶液












