有—处于平衡状态的反应: 正反应放热。为使平衡状态向生成E的方向移动 适宜的条件是①高温 ②低温
有—处于平衡状态的反应: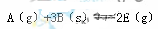 ,正反应放热。为使平衡状态向生成E的方向移动,适宜的条件是①高温、②低温、③高压、④低压、⑤加催化剂、⑥将E ,正反应放热。为使平衡状态向生成E的方向移动,适宜的条件是①高温、②低温、③高压、④低压、⑤加催化剂、⑥将E分离除去 ( )
|
参考解答
| B |
因为正反应为放热反应,所以为使平衡向生成Z的方向移动,可以降低反应温度①错,②对; 因为该反应是体积减小的反应,所以为使平衡向生成Z的方向移动,可以增大压强,③对,④错。(对该反应增大压强,平衡向气体体积减小的方向移动) 催化剂不改变平衡的移动,只改变反应速率; 对于⑥: 若分离出的是反应物Y(g),则平衡向逆向移动; 若分离出的是Z(g)平衡向正向移动; 若分离出的是X(s)平衡不移动,因为其为固体。 故选B,而非题目给出的C。 |
相似问题
在一体积可变的密闭容器中 通入1molN2和3 mol H2 发生反应 在t1时刻达到平衡。保持温度
在一体积可变的密闭容器中,通入1molN2和3 mol H2,发生反应,在t1时刻达到平衡。保持温度和压强不变,在t2时刻,再通入一部分NH3,反应速率(v)与时间(
某温度下 在密闭容器中存在下列可逆反应:A(g)+2B(g) 4 C(g) 达到平衡时 各物质的
某温度下,在密闭容器中存在下列可逆反应:A(g)+2B(g) 4 C(g),达到平衡时,各物质的物质的量之比为n(A)∶n(B)∶n(C)=2∶2∶1,且A的质量分数为w%。保
在一定条件下 密闭容器中可发生可逆反应:N2(g) + 3H2(g) 2NH3(g) 。下列说法中
在一定条件下,密闭容器中可发生可逆反应:N2(g) + 3H2(g) 2NH3(g) 。下列说法中,表明这一反应已经达到化学平衡状态的是A.N2、H2、NH3的浓度相等B
(7分)在0.1L密闭容器中有0.1molSO2和0.05molO2发生反应 恒温下30min后达到
(7分)在0 1L密闭容器中有0 1molSO2和0 05molO2发生反应,恒温下30min后达到平衡。(1)若得到0 06molSO3,求达平衡时SO2的浓度;(2)求30min内的反应
一定温度下恒容的密闭容器中 反应A2(g)+B2(g) 2AB(g)达到平衡的标志是A.正反应速率和
一定温度下恒容的密闭容器中,反应A2(g)+B2(g) 2AB(g)达到平衡的标志是A.正反应速率和逆反应速率相等且都为零B.容器内气体的总压强不随时间变化C.单












