右图所示为800 ℃ 时A B C三种气体在密闭容器中反应时浓度的变化 只从图上分析不能得出的结论是
| 右图所示为800 ℃ 时A、B、C三种气体在密闭容器中反应时浓度的变化,只从图上分析不能得出的结论是( ) A.A是反应物 B.前2 min A的分解速率为0. 1 mol·L-1·min-1 C. 达平衡后,若升高温度,平衡向正反应方向移动 D.反应的方程式为:2A (g) 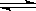 2 B(g) + C(g) 2 B(g) + C(g) 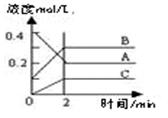 |
参考解答
| C |
A正确,由图得A的浓度逐渐减少,所以为反应物;B正确,反应速率为单位时间内反应物浓度的减少或生成物浓度的增加;C错,因该反应是放热反应还是吸热反应不知;D正确,根据变化的量比等于化学计量数比得2A (g) 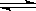 2 B(g) + C(g); 2 B(g) + C(g); |
相似问题
(6分)将和在适宜条件下按下式进行反应 当在某一温度下达到化学平衡状态 试解答: (1)若测得平衡
(6分)将和在适宜条件下按下式进行反应,当在某一温度下达到化学平衡状态,试解答: (1)若测得平衡混合气体对空气的相对密度为0 6时,求的转化率.
一定温度下 有可逆反应:2A(g)+2B(g)C(g)+3D(g)ΔH<0。现将2molA和2mol
一定温度下,有可逆反应:2A(g)+2B(g)C(g)+3D(g)ΔH<0。现将2molA和2molB充入体积为V的甲容器,将2molC和6molD充入乙容器并使乙容器在反应开
在一体积为1L的容器中 通入一定量的N2O4 在100℃时发生如下反应 N2O42NO2–Q(Q>0
在一体积为1L的容器中,通入一定量的N2O4,在100℃时发生如下反应,N2O42NO2–Q(Q>0),其N2O4和NO2浓度变化如图如示。(1)上述反应的平衡常数表达式为
在密闭容器中的一定量混合气体发生反应xA(g)+yB(g)zC(g) 平衡时测得A的浓度为0.50m
在密闭容器中的一定量混合气体发生反应xA(g)+yB(g)zC(g),平衡时测得A的浓度为0 50mol L 保持温度不变,将容器的容积扩大到原来的两倍时测得A的浓度降低
(10分)恒温恒容下 将2mol A气体和2mol B气体通人体积为2L的密闭容器中发生如下反应:2
(10分)恒温恒容下,将2mol A气体和2mol B气体通人体积为2L的密闭容器中发生如下反应:2A(g)+B(g)xC(g)+2D(s),2min时反应达到平衡状态.此












