Ⅰ.在一体积为10 L的容器中 通入一定量的CO和H2O 在850℃时发生如下反应:CO(g)+H2
Ⅰ.在一体积为10 L的容器中,通入一定量的CO和H2O,在850℃时发生如下反应:CO(g)+H2O(g) CO2(g)+H2(g) ΔH<0,CO和H2O浓度变化如图所示: CO2(g)+H2(g) ΔH<0,CO和H2O浓度变化如图所示:(1)0~4 min的平均反应速率v(CO)=________mol/(L·min),反应在第5 min时的平衡常数K=________。  t℃时物质浓度(mol/L)的变化
(2)t℃(高于850℃)时,在相同容器中发生上述反应,容器内各物质的浓度变化如表所示: ①表中3~4 min之间反应处于________状态;c1数值________(填“>”“=”或“<”)0.08 mol/L。 ②反应在4~5 min间,平衡向逆反应方向移动,可能的原因是________(填标号,下同),表中5~6 min之间数值发生变化,可能的原因是________。 A.增加水蒸气B.降低温度C.使用催化剂D.增加氢气浓度 Ⅱ.在热的稀硫酸中溶解了11.4 g硫酸亚铁固体,当加入50 mL 0.5 mol/L的KNO3溶液后,使其中的Fe2+全部转化成Fe3+、KNO3也完全反应并放出NxOy气体。 (3)推算出x=________,y=________。 (4)写出该反应的化学方程式:________________(x、y用具体数值表示)。 (5)反应中氧化产物是________。 |
参考解答
| (1)0.03 1 (2)①平衡 > ②D A (3)1 1 (4)6FeSO4+2KNO3+4H2SO4=K2SO4+3Fe2(SO4)3+2NO↑+4H2O (5)Fe2(SO4)3 |
Ⅰ.(1)0~4 min的平均速率v(CO)=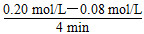 =0.03 mol/(L·min);由图示知平衡时H2O、CO、CO2、H2的浓度分别为0.18 mol/L、0.12 mol/L、0.12 mol/L,故平衡常数K= =0.03 mol/(L·min);由图示知平衡时H2O、CO、CO2、H2的浓度分别为0.18 mol/L、0.12 mol/L、0.12 mol/L,故平衡常数K=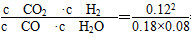 =1。(2)①在3~4 min内,各物质的浓度不再变化,因此反应处于化学平衡状态;因正反应为放热反应,故升温平衡向逆反应方向进行,故c1的数值大于0.08 mol/L。②增加水蒸气、降温则反应向正反应方向进行;加入催化剂平衡不移动;加入氢气,平衡向逆反应方向移动;利用表中数据知在4~5 min时,改变的条件是增加H2浓度,在5~6 min时,改变的条件是增加水蒸气,平衡向正反应方向移动引起的数据变化。 =1。(2)①在3~4 min内,各物质的浓度不再变化,因此反应处于化学平衡状态;因正反应为放热反应,故升温平衡向逆反应方向进行,故c1的数值大于0.08 mol/L。②增加水蒸气、降温则反应向正反应方向进行;加入催化剂平衡不移动;加入氢气,平衡向逆反应方向移动;利用表中数据知在4~5 min时,改变的条件是增加H2浓度,在5~6 min时,改变的条件是增加水蒸气,平衡向正反应方向移动引起的数据变化。Ⅱ.设放出气体NxOy中N的化合价为+a价,由得失电子守恒可知(5-a)×0.05 L×0.5 mol/L= 11.4 g÷152 g·mol-1,解得a=2,即放出气体为NO,因此x=y=1。 点拨:本题考查化学平衡、氧化还原反应,考查考生的理解能力、计算能力。难度中等。 |
相似问题
ClO2是一种消毒杀菌效率高的消毒剂 有强氧化性。工业上ClO2常用NaClO3和Na2SO3溶液混
ClO2是一种消毒杀菌效率高的消毒剂,有强氧化性。工业上ClO2常用NaClO3和Na2SO3溶液混合并加H2SO4酸化后反应制得。则有关此反应的说法正确的是()A.NaC
标出下列反应电子转移的方向和数目2KMnO4+16HCl(浓)==2KCl+2MnCl2+5Cl2↑
标出下列反应电子转移的方向和数目2KMnO4+16HCl(浓)==2KCl+2MnCl2+5Cl2↑+8H2O其中氧化剂的是,每生成1mol Cl2,电子转移了mol。
下列两个反应均为在溶液中进行的反应 试按下列要求作答:①在表格中填出反应式中的氧化剂 还原剂 氧化产
下列两个反应均为在溶液中进行的反应,试按下列要求作答:①在表格中填出反应式中的氧化剂、还原剂,氧化产物、还原产物。②将其改写成离子方程式;(1)
已知R有多种化合价 其最高正价为+7价。在一定条件下 RO3-与R-可发生反应:RO3-+5R-+6
已知R有多种化合价,其最高正价为+7价。在一定条件下,RO3-与R-可发生反应:RO3-+5R-+6H+=3R2+3H2O,下列关于R元素的叙述中,正确的是()A.元素R位
2005年诺贝尔化学奖获得者施罗克等人发现 金属钼的卡宾化合物可以作为非常有效的烯烃复分解催化剂。工
2005年诺贝尔化学奖获得者施罗克等人发现,金属钼的卡宾化合物可以作为非常有效的烯烃复分解催化剂。工业上冶炼钼的化学原理为()①2MoS2+7O22MoO3+4SO2












