在水溶液中 YO3-与S2-发生反应的离子方程式为:YO3-+3S2-+6H+=Y-+3S↓+3H2
| 在水溶液中,YO3-与S2-发生反应的离子方程式为:YO3-+3S2-+6H+=Y-+3S↓+3H2O. 请回答: (1)此反应中,氧化剂是______;Y元素原子的最外层电子数是______. (2)请表示此反应的电子转移的方向和数目:______. |
参考解答
| (1)在反应YO3-+3S2-+6H+=Y-+3S↓+3H2O中,Y元素的化合价降低,所以Y所在的反应物YO3-是氧化剂,在YO3-中Y元素的化合价是+5价,Y的最低化合价为-1价,说明Y得1个电子达到饱和,最外层应有7个电子, 故答案为:YO3-,7; (2)此反应中Y元素化合价降低,的电子,S元素化合价升高,失去电子,化合价降低值=化合价升高值=反应中转移的电子数目=6,电子转移的方向和数目表示为: 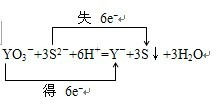 , 故答案为:  . |
相似问题
实验室用MnO2与浓HCl制取Cl2:MnO2+4HCl(浓) △ . MnCl2+Cl2↑+2
实验室用MnO2与浓HCl制取Cl2:MnO2+4HCl(浓)△ MnCl2+Cl2↑+2H2O,下列说法正确的是( )A.MnO2作氧化剂,发生氧化反应,MnCl2是氧化产物B.在反应
关于反应KClO3+6HCl(浓)═2KCl+3Cl2↑+3H2O 的说法中正确的是( )A.HC
关于反应KClO3+6HCl(浓)═2KCl+3Cl2↑+3H2O的说法中正确的是( )A.HCl发生还原反应B.产生3molCl2时转移5摩尔电子C.+5价的氯转变为-1价的氯D.氧
现有反应:①CO+CuO 加热 . Cu+CO2 ②MgO+2HCl=MgCl2+H2O
现有反应:①CO+CuO加热 Cu+CO2②MgO+2HCl=MgCl2+H2O③Cu+2AgNO3=Cu(NO3)2+2Ag④CH4+2O2点燃 CO2+2H2O⑤NH4HCO3加热 NH3↑+CO2↑+H2O试回答:(1)上述
对于反应2MnO-4+5H2C2O4+6H+═10CO2↑+2Mn2+8H2O 下列分析错误的是(
对于反应2MnO-4+5H2C2O4+6H+═10CO2↑+2Mn2+8H2O,下列分析错误的是( )A.该反应氧化剂是H2C2O4B.反应中1mo1MnO-4得到5NA个e-C.该反应的还原产物
向一定量的浓硝酸里①加入过量的铜 开始反应发生的化学方程式______反应一段时间后 硝酸浓度会变稀
向一定量的浓硝酸里①加入过量的铜,开始反应发生的化学方程式______反应一段时间后,硝酸浓度会变稀,反应的离子方程式______反应中硝酸的作用是______












