提纯某KCl样品(含有少量的MgCl2和K2SO4)的方案(所加试剂均过量)如下:样品溶液浊液滤液溶
| 提纯某KCl样品(含有少量的MgCl2和K2SO4)的方案(所加试剂均过量)如下: 样品 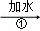 溶液 溶液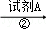 浊液 浊液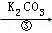 滤液 滤液 溶液 溶液回答下列问题: (1)步骤①和③的实验操作均用到的玻璃仪器有玻璃棒和 . (2)步骤②得到的浊液中含有Mg(OH)2和BaSO4沉淀,写出生成BaSO4的化学方程式 . (3)确定步骤③所加的K2CO3是否过量的方法是:在加入K2CO3后的浊液中取少量上层澄清液于试管,然后滴加K2CO3溶液,若没有白色沉淀生成,则说明所加K2CO3 . (4)步骤④得到的溶液的溶质除了KCl外,还含有 (填化学式).若要得到KCl晶体,还要进行如下操作:将溶液倒入 (填仪器名称)中,加热蒸发并用玻璃棒不断搅拌,直到 时(填现象),停止加热,用余热使水分蒸干. |
参考解答
| (1)烧杯 (2)Ba(OH)2+K2SO4═BaSO4↓+2KOH (3)过量 (4)HCl 蒸发皿 出现较多固体 |
试题分析:(1)溶解、过滤时都要用到玻璃棒和烧杯. 故填:烧杯. (2)步骤②得到的浊液中含有Mg(OH)2和BaSO4沉淀,说明试剂A是氢氧化钡溶液,氢氧化钡和硫酸钾反应能生成硫酸钡沉淀和氢氧化钾,反应的化学方程式为: Ba(OH)2+K2SO4═BaSO4↓+2KOH. 故填:Ba(OH)2+K2SO4═BaSO4↓+2KOH. (3)在加入K2CO3后的浊液中取少量上层澄清液于试管,然后滴加K2CO3溶液,若没有白色沉淀生成,则说明所加碳酸钾过量. 故填:过量. (4)步骤④得到的溶液的溶质除了KCl外,还含有盐酸,盐酸中的溶质是氯化氢,化学式是HCl. 故填:HCl. 蒸发结晶时,用到的仪器是蒸发皿. 故填:蒸发皿. 加热蒸发并用玻璃棒不断搅拌,直到出现较多固体时,停止加热,用余热使水分蒸干. 故填:出现较多固体. 点评:本题主要考查杂质的去除、化学方程式的书写、蒸发结晶等方面的知识,要注意蒸发结晶操作过程中,停止加热的时间要掌握好. |
相似问题
某固体混合物由K2CO3 K2SO4 CaCl2和KCl中的一种或几种组成 实验记录如下:①取该样品
某固体混合物由K2CO3、K2SO4、CaCl2和KCl中的一种或几种组成,实验记录如下:①取该样品溶于水,得到无色溶液;②取适量上述溶液滴加过量的BaCl2溶液,出
A B C D E是初中化学常见的不同类别的物质(物质按单质 氧化物 酸 碱 盐分类) 已知A是单
A、B、C、D、E是初中化学常见的不同类别的物质(物质按单质、氧化物、酸、碱、盐分类), 已知A是单质,C是红棕色固体。它们之间的转化关系如下(“—”
下表除去杂质的方法中 正确的是( )选项物质(括号内为杂质)除去杂质的方法ACu(NO3)2溶液(
下表除去杂质的方法中,正确的是( )选项物质(括号内为杂质)除去杂质的方法ACu(NO3)2溶液(AgNO3)加过量铜粉,过滤BKCl溶液(CaCl2)加适量Na2CO3
有A.B.C.D.E.F.G.H初中常见的八种物质 常温下A和B是液体 D.E.G是气体 A和B D
有A B C D E F G H初中常见的八种物质,常温下A和B是液体,D E G是气体,A和B,D和G组成元素相同;EFH是单质,且F为金属,八种物质之间的转化如下图所示,
小阳同学在厨房里 发现3包用相同塑料袋装着的白色粉末 询问后得知是淀粉 苏打(碳酸钠 Na2CO3)
小阳同学在厨房里,发现3包用相同塑料袋装着的白色粉末,询问后得知是淀粉、苏打(碳酸钠、Na2CO3)和小苏打(碳酸氢钠、NaHCO3).为了区分它们,把3种












