X Y Z为不同短周期非金属元素的气态单质.在一定条件下能发生如下反应:Y+X→甲(g) Y+Z→乙
| X、Y、Z为不同短周期非金属元素的气态单质.在一定条件下能发生如下反应:Y+X→甲(g),Y+Z→乙(g).甲、乙可化合生成离子化合物,甲的相对分子质量小于乙. (1)X的结构式是______. (2)磷在Z气体中燃烧可生成液态丙分子,也可生成固态丁分子.已知丙分子中各原子最外层均是8电子结构,丙的电子式是______.磷单质和Z单质反应生成1mol丙时,反应过程与能量变化如图Ⅰ所示,该反应的热化学方程式是______. (3)某同学拟用图Ⅱ所示装置证明氧化性Z>I2,已知高锰酸钾与乙的浓溶液反应生成Z,则a是______的水溶液.若仅将a换为甲的浓溶液,实验时会产生大量白烟并有气体单质生成,该反应的化学方程式是______. (4)向一定浓度的BaCl2溶液中通入SO2气体,未见沉淀生成,若在通入SO2气体的同时加入由X.Y.Z|中的一种或几种元素组成的某纯净物,即可生成白色沉淀,该纯净物可能是______、______. 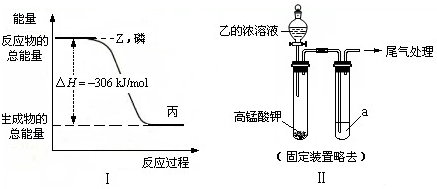 |
参考解答
| X、Y、Z为不同短周期非金属元素的气态单质,Y+X→甲(g),Y+Z→乙(g).甲、乙可化合生成离子化合物,则该化合物为NH4Cl,甲的相对分子质量小于乙,则甲为NH3,乙为 HCl,Y为H2,X为N2,Z为Cl2, (1)X为N2,氮原子之间有3对共用电子对,结构为N≡N,故答案为:N≡N; (2)P在氯气中燃烧可生成PCl3或PCl5,其中PCl3分子中各原子最外层均是8电子结构,电子式为 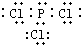 , 根据图象可知 P(s)+
P(s)+
故答案为: 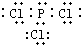 ; P(s)+
(3)氯气的氧化性大于碘的氧化性,将氯气通入淀粉KI溶液中生成碘单质,溶液变蓝,氯气具有强氧化性,与过量氨气反应生成NH4Cl和N2,反应的方程式为8NH3+3Cl2=6NH4Cl+N2, 故答案为:淀粉KI或KI;8NH3+3Cl2=6NH4Cl+N2; (4)若在通入SO2气体的同时加入Cl2,发生反应为SO2+Cl2+2H20═H2SO4+2HCl,在BaCl2溶液中生成BaSO4沉淀,若在通入SO2气体的同时加入NH3,溶液中存在大量的SO3-,可生成沉淀 BaSO3,故答案为:Cl2; NH3. |
相似问题
工业上从硒的废料中提取硒的方法之一是用H2SO4和NaNO3处理废料 获得亚硒酸和少量硒酸。加入盐酸
工业上从硒的废料中提取硒的方法之一是用H2SO4和NaNO3处理废料,获得亚硒酸和少量硒酸。加入盐酸共热,硒酸被转化为亚硒酸(2HCl+H2SeO4==H2SeO3+Cl2+H2O)
已知反应2X-+Z2=2Z-+X2 2W-+X2=2X-+W2能从左向右进行 则反应:W2+2Z-=
已知反应2X-+Z2=2Z-+X2,2W-+X2=2X-+W2能从左向右进行,则反应:W2+2Z-=Z2+2W-进行的方向是( )A.从左向右B.从右向左C.不能进行D.无法判断
下列四组物质反应 其中与其它三组有本质不同的是A.Na2O2 + H2OB.Cl2 + H2O C.
下列四组物质反应,其中与其它三组有本质不同的是A.Na2O2 + H2OB.Cl2 + H2O C.F2 + H2O D.NO2 + H2O
根据下列反应 有关离子的还原性强弱顺序正确的是( )①2Fe3++2I-=2Fe2++I2②2Fe
根据下列反应,有关离子的还原性强弱顺序正确的是( )①2Fe3++2I-=2Fe2++I2②2Fe2++Br2=2Fe3++2Br-.A.Br->I->Fe2+B.Fe2+>I->Br-C.Br->Fe2+>I-D.I->Fe2+>Br-
(1)某学生用KMnO4制备氯气 反应方程式如下:2KMnO4 + 16HCl = 2KCl + 2
(1)某学生用KMnO4制备氯气,反应方程式如下:2KMnO4 + 16HCl = 2KCl + 2MnCl 2+ 5Cl 2↑+ 8H2O当有15 8g KMnO4参加反应时,消耗molHCl












