(1)已知钾有多种氧化物:普通氧化物 过氧化物 超氧化物和臭氧化物等。标出下列钾的氧化物中氧的化合价
| (1)已知钾有多种氧化物:普通氧化物、过氧化物、超氧化物和臭氧化物等。标出下列钾的氧化物中氧的化合价: K2O________________,K2O2:________________,KO2:________________,KO3:_____________。 (2)过氧化钾与过氧化钠性质类似,是强氧化剂,也是生氧剂,试分别写出K2O2与CO2和H2O(g)反应的化学方程式: ________________________________________、____________________________________。 (3)超氧化钾是更强的氧化剂和生氧剂,试分别写出超氧化钾(KO2)与CO2和H2O(g)反应的化学方程式(都是歧化反应): _________________________________________、___________________________________。 |
参考解答
| (1):-2 -1 -1/2 -1/3 (2)2K2O2+2CO2====2K2CO3+O2 2K2O2+2H2O====4KOH+O2↑ (3)4KO2+2CO2====2K2CO3+3O2 4KO2+2H2O====4KOH+3O2↑ |
(1)设K2O、K2O2、KO2、KO3中氧元素的化合价分别为x、y、z、ω。由于化合物中正、负化合价的代数为0,所以: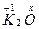 :+1×2+x=0,x=-2; :+1×2+x=0,x=-2;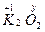 :+1×2+2y=0,y=-1; :+1×2+2y=0,y=-1;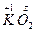 :+1+2z=0,z=-1/2; :+1+2z=0,z=-1/2;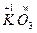 K+1Ow3:+1+3ω=0,ω=-1/3。 K+1Ow3:+1+3ω=0,ω=-1/3。(2)K2O2与Na2O2的组成和结构相似,类比Na2O2与CO2和H2O的反应,可写出K2O2与CO2和H2O的反应: 2Na2O2+2CO2====2Na2CO3+O2 2Na2O2+2H2O====4NaOH+O2↑ 2K2O2+2CO2====2K2CO3+O2 2K2O2+2H2O====4KOH+O2 (3)由于KO2与CO2和H2O的反应都是歧化反应,所以CO2和H2O中各元素的化合价反应前后未变。由于KO2是生氧剂,所以有O2生成,则另一产物是K2CO3或KOH。 2KO2+1CO2====1K2CO3+ 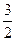 O2 O22KO2+1H2O====2KOH+ 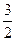 O2 O2计量数都乘以2得: 4KO2+2CO2====2K2CO3+3O2 4KO2+2H2O====4KOH+3O2 |
相似问题
某同学欲探究Na2O2与水的反应 可供使用的试剂有:Na2O2 蒸馏水 KMnO4酸性溶液 MnO2
某同学欲探究Na2O2与水的反应,可供使用的试剂有:Na2O2、蒸馏水、KMnO4酸性溶液、MnO2.该同学取一定量Na2O2样品与过量水反应,待完全反应后,得到溶液X
某种混合气体 可能含有N2 HCl CO。把混合气体依次通过足量的NaHCO3溶液和灼热的CuO 气
某种混合气体,可能含有N2、HCl、CO。把混合气体依次通过足量的NaHCO3溶液和灼热的CuO,气体体积都没有变化;再通过足量的Na2O2固体,气体体积变小;最后
下列物质露置在空气中 质量会减轻的是( )A.NaOHB.Na2O2C.无水CaCl2D.Na2
下列物质露置在空气中,质量会减轻的是()A.NaOHB.Na2O2C.无水CaCl2D.Na2CO3·10H2O
电子工业制造光电管时 需要一种经强光照射就失去电子 从而接通电路的材料。制造这种材料的物质应该是(
电子工业制造光电管时,需要一种经强光照射就失去电子,从而接通电路的材料。制造这种材料的物质应该是()A.放射性元素B.超铀元素C.活泼非金属元素D
俗名和化学式符合的是( )①纯碱NaCl ②苛性钠Na ③苏打NaHCO3 ④烧碱 NaOH⑤芒
俗名和化学式符合的是()①纯碱NaCl②苛性钠Na③苏打NaHCO3④烧碱 NaOH⑤芒硝Na2SO4·10H2OA.①②B.③④C.②③D.④⑤












