如图所示 当关闭K时 向A中充入4molX 14molY 向B中充入2molX 7molY 起始时V
如图所示,当关闭K时,向A中充入4molX、14molY,向B中充入2molX、7molY,起始时V(A)=V(B)=a升,在相同温度和有催化剂存在的条件下,两容器各自发生下列反应:2X(g)+2Y(g) Z(g)+2W(g) △H<0。达到平衡(Ⅰ)时,B中密度变为原来的 Z(g)+2W(g) △H<0。达到平衡(Ⅰ)时,B中密度变为原来的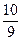 ,试回答: ,试回答: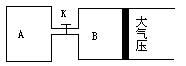 (1)设A、B两容器中化学平衡常数分别为K1和K2,则它们的大小关系是K1____K2(填“大于”或“等于”或“小于”)。 (2)B中X的转化率α(X)B为 。 (3)A中Z和B中的W物质的量的比较: n(Z)A n(W)B(填“大于”或“等于”或“小于”)。 (4)打开K,过一段时间重新达平衡(Ⅱ)时,B的体积为 升(用含a的代数式表示,连通管中气体体积不计);在温度不变的情况下,要使B容器恢复原来反应前的体积,可采取的措施是 。 |
参考解答
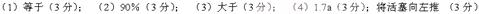 |
| 略 |
相似问题
C+CO2 2CO(正反应吸热) 反应速率为v1:N2+3H2 2NH3(正反应放热) 反应速率为
C+CO2 2CO(正反应吸热),反应速率为v1:N2+3H22NH3(正反应放热),反应速率为v2。对于上述反应,当温度降低时,v1和v2的变化情况是()A.同时增大
下列事实能用勒夏特列原理解释的是A.合成氨工业采用高温条件B.配制FeSO4溶液时在溶液中加入稀硫酸
下列事实能用勒夏特列原理解释的是A.合成氨工业采用高温条件B.配制FeSO4溶液时在溶液中加入稀硫酸C.H2、I2、HI 平衡混合气体加压后颜色变深D.工业制
(8分)将等物质的量的A B混合于2 L的密闭容器中 发生如下反应:3A(g)+B(g) xC(g)
(8分)将等物质的量的A、B混合于2 L的密闭容器中,发生如下反应:3A(g)+B(g)xC(g)+2D(g),经5 min后达平衡状态,此时测得D的浓度为0 5 mol L,混合气
(10分).随着人类对温室效应和资源短缺等问题的重视 如何降低大气中CO2的含量及有效地开发利用CO
(10分).随着人类对温室效应和资源短缺等问题的重视,如何降低大气中CO2的含量及有效地开发利用CO2,引起了各国的普遍重视。⑴目前工业上有一种方法是
在一个固定容积的密闭容器中 可逆反应N2+3H22NH3达到平衡的标志是A.v(N2)正= v(NH
在一个固定容积的密闭容器中,可逆反应N2+3H22NH3达到平衡的标志是A.v(N2)正= v(NH3)逆B.单位时间内3 mol H-H断键反应,同时2 mol N-H也断键反应C












