将铁粉和铜粉的混合物7g 加入到盛有58.1g稀盐酸的烧杯中 恰好完全反应.此时烧杯内各物质的总质量
| 将铁粉和铜粉的混合物7g,加入到盛有58.1g稀盐酸的烧杯中,恰好完全反应.此时烧杯内各物质的总质量为64.9g.试计算: (1)原混合物中铁粉的质量分数; (2)反应后所得溶液中溶质的质量分数; (3)配制上述反应中所用稀盐酸需要质量分数为38%的浓盐酸(密度为1.19g/cm3)的体积.(计算结果精确到0.1) |
参考解答
答案:
(1)80%
(2)20%
(3)16.1cm3
解析:反应后生成氢气的质量为:7g+58.1g-64.9g=0.2g
设生成0.2g氢气需要铁粉的质量为x,同时生成FeCl2的质量为y。
Fe+2HCl= FeCl2+H2↑
56 127 2
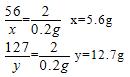
(1)原混合物中铁粉的质量分数为![]()
(2)反应后所得溶液中溶质的质量分数为![]()
(3)设配制上述反应中所用稀盐酸需要质量分数为38%的浓盐酸(密度为1.19g/cm3)的体积为z,
1.19g/cm3×z×38%=0.2g+12.7g-5.6g,解得z=16.1cm3
相似问题
烧杯中装有一定量硫酸和硫酸铜的混合溶液 若向该溶液中加入足量的BaCl2溶液 产生46.6克沉淀;若
烧杯中装有一定量硫酸和硫酸铜的混合溶液,若向该溶液中加入足量的BaCl2溶液,产生46 6克沉淀;若向该溶液中加入10%的NaOH溶液,得到沉淀的质量记录如下
用20克的KMnO4加热制氧气 制得所需氧气后 停止加热 称取剩余固体质量为18.72克.问:①制取
用20克的KMnO4加热制氧气,制得所需氧气后,停止加热,称取剩余固体质量为18 72克.问:①制取氧气______克.②消耗了多少克的KMnO4?
某化学活动小组用化学方法测定一种钢样品中铁的含量.同学们称取了5.7g钢样品 投入装有50.0g稀盐
某化学活动小组用化学方法测定一种钢样品中铁的含量.同学们称取了5 7g钢样品,投入装有50 0g稀盐酸(足量)的烧杯中(烧杯质量也为50 0g,样品中杂质不
用15.8g KMnO4与12mol/L的 浓HCl发生.反应方程式如下:2KMnO4+16HCl=
用15 8gKMnO4与12mol L的浓HCl发生.反应方程式如下:2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O通过计算解答以下问题:(1)KMnO4能使多少毫升浓HCl发生上述
我国铁矿石资源比较丰富 2000年 钢铁年总产量就已达到1.27亿吨 成为世界钢铁大国.某钢铁厂日产
我国铁矿石资源比较丰富,2000年,钢铁年总产量就已达到1 27亿吨,成为世界钢铁大国.某钢铁厂日产含3%杂质的生铁2240t,则需要含Fe2O380%的赤铁矿多少吨?












