(1)氨气易溶于水生成氨水 氨水电离生成铵根离子 铵根离子中氮原子采取________杂化 NH4+
| (1)氨气易溶于水生成氨水,氨水电离生成铵根离子,铵根离子中氮原子采取________杂化,NH4+中H—N—H键角比NH3中H—N—H键角大,原因是__________________。 (2)Cu3N形成的晶体结构如图所示,N3-的配位数是________________。 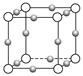 (3)常温常压下,给水施加一个弱电场便可形成冰,称之为“热冰”,热冰中微粒间存在的作用力有________,其大小顺序是__________。 (4)NaF和NaCl属于同一主族的钠盐,但NaF的莫氏硬度比NaCl大,原因是__________。 |
参考解答
| (1)sp3 氨气分子中氮原子上有一对孤电子对,铵根离子中氮原子上没有孤电子对,排斥力小 (2)6 (3)化学键、范德华力、氢键 化学键>氢键>范德华力 (4)相同类型的离子晶体,晶格能与离子半径成反比,离子晶体的晶格能越大,其莫氏硬度越大,氟离子半径小于氯离子半径,所以氟化钠的晶格能大于氯化钠,则NaF的莫氏硬度比NaCl大 |
| (1)铵根离子中含有4个键,没有孤电子对,氮原子采取sp3杂化,氨气分子中氮原子上有一对孤电子对,铵根离子中氮原子上没有孤电子对,排斥力小。 (2)○∶8× 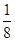 =1 =1 ∶12× ∶12×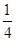 =3 =3所以○代表N3-,  代表Cu+ 代表Cu+N3-的配位数为6(上下、前后、左右)。 (3)热冰中微粒间存在的作用力有化学键、范德华力、氢键,微粒间作用力大小顺序是化学键>氢键>范德华力。 (4)相同类型的离子晶体,晶格能与离子半径成反比,离子晶体的晶格能越大,其莫氏硬度越大,氟离子半径小于氯离子半径,所以氟化钠的晶格能大于氯化钠,则NaF的莫氏硬度比NaCl大。 |
相似问题
下列原子中有21个中子的是[ ]A.147N B.2110NeC.4019K D.4521S
下列原子中有21个中子的是[ ]A.147N B.2110NeC.4019K D.4521Se
下列各选项中两种粒子所含电子数不相等的是[ ]A.羟基(-OH)和氢氧根(OH-)B.甲烷(
下列各选项中两种粒子所含电子数不相等的是[ ]A.羟基(-OH)和氢氧根(OH-)B.甲烷(CH4)和铵根(NH4+) C.氨气(NH3)和水(H2O)D.双氧水(H2O2)氯化氢(HCl)
下列对分子或离子的立体构型判断不正确的是 ( )。A.NH4+和CH4都是正四面体形B.CO2和
下列对分子或离子的立体构型判断不正确的是 ( )。A.NH4+和CH4都是正四面体形B.CO2和CS2都是直线形C.NCl3和BCl3都是三角锥形D.H2O和H2S都是V形
气体分子中的极性键在红外线的照射下 易像弹簧一样做伸缩和弯曲运动 从而产生热量而造成温室效应。下列不
气体分子中的极性键在红外线的照射下,易像弹簧一样做伸缩和弯曲运动,从而产生热量而造成温室效应。下列不属于温室效应气体的是( )A.CO2B.N2O C.CH4D.N2
据报道 最近中科院的有关专家在世界上首次发现了镤元素的一种新的同位素 它的中子数为[ ]A.
据报道,最近中科院的有关专家在世界上首次发现了镤元素的一种新的同位素,它的中子数为[ ]A.330 B.91 C.239 D.148












