按右图装置实验 用惰性电极电解足量的NaOH溶液和足量CuSO4溶液.通电一段时间后 c极上有6.4
| 按右图装置实验,用惰性电极电解足量的NaOH溶液和足量CuSO4溶液.通电一段时间后,c极上有6.4gCu析出. (1)电源P为______极; (2)b极产生气体的体积为______L(标准状况); (3)A烧杯溶液PH变化______(增大、减小或不变 ) (4)d极上所发生的电极反应式______,B烧杯总反应的化学方程式______.若要使B中溶液恢复电解前的状态,可向溶液中加入______(填写物质的化学式)______g. 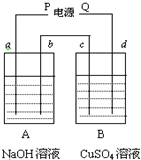 |
参考解答
| (1)B杯中c质量增加,说明Cu沉积在c电极上,所以c是阴极,d是阳极,即Q为正极,P为负极,故答案为:负; (2)P是负极,所以a是阴极,b是阳极,b极上的电极反应为:4OH--4e-=2H2O+O2↑,c极上的电极反应为:Cu2++2e-=Cu,整个电路是串联的,所以每个烧杯中的电极上转移电子数是相等的,据电极反应:Cu2++2e-=Cu,可知c极上有6.4gCu析出,转移0.2mol电子,当转移0.2mol电子时,b极上生成氧气的物质的量为0.05mol,体积为0.05mol×22.4L/mol=1.12L.故答案为:1.12; (3)A烧杯溶液电解的实质是电解水,所以氢氧化钠溶度增大,PH变大,故答案为:增大; (4)d是阳极,电解硫酸铜时,在阳极上是氢氧根离子放电,电极反应式为:4OH--4e-=2H2O+O2↑,总的电解原理方程式为:2CuSO4+2H2O
故答案为:4OH--4e-=2H2O+O2↑;2CuSO4+2H2O
|
相似问题
电解装置如图所示 电解槽内装有KI及淀粉溶液 中间用阴离子交换膜隔开.在一定的电压下通电 发现左侧溶
电解装置如图所示,电解槽内装有KI及淀粉溶液,中间用阴离子交换膜隔开.在一定的电压下通电,发现左侧溶液变蓝色,一段时间后,蓝色逐渐变浅.已知:3I2
将0.1L含有0.02mol CuSO4和0.01mol NaCl的水溶液用惰性电极电解.电解一段时
将0 1L含有0 02molCuSO4和0 01molNaCl的水溶液用惰性电极电解.电解一段时间后,某电极的质量增加了0 64g.下列说法正确的是( )A.质量增加的电极为
下列关于电解的说法正确的是 [ ]A. 工业上通常用电解饱和食盐水生产金属钠 电解熔融氯化铝
下列关于电解的说法正确的是 [ ]A 工业上通常用电解饱和食盐水生产金属钠,电解熔融氯化铝冶炼铝 B 电镀时,通常把待镀的金属制品做阳极 C 电解法精
以惰性电极电解100mL 0.1mol?L-1CuSO4溶液.若阳极上产生气体的物质的量为0.01m
以惰性电极电解100mL0 1mol?L-1CuSO4溶液.若阳极上产生气体的物质的量为0 01mol,则阴极上析出Cu的质量为( )A.0 32gB.0 64gC.1 28gD.2 56g
用石墨作电极电解2 mol·L-1NaCl和1 mol·L-1MgSO4混合溶液时 下列曲线合理的是
用石墨作电极电解2 mol·L-1NaCl和1 mol·L-1MgSO4混合溶液时,下列曲线合理的是 [ ]A B C D












