据国家标准 碳铵化肥中NH4HCO3含量不得低于95%.某同学利用如图装置和如下反应进行了三次实验(
| 据国家标准,碳铵化肥中NH4HCO3含量不得低于95%.某同学利用如图装置和如下反应进行了三次实验(假设杂质不发生反应): NH4HCO3
2NH3+H2SO4═(NH4)2SO4 实验结果如下:
(2)这个结果能否说明这种化肥合格与否,请说明原因. 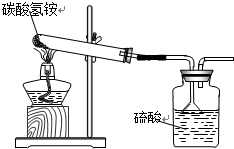 |
参考解答
| (1)设参与反应的NH4HCO3质量为x, NH4HCO3=NH3↑+H2O+CO2↑ 79 17 x 1.7g
解之得:x=7.9g; 该化肥中碳酸氢铵的质量分数为:
(2)这个结果不能说明这种化肥合格,因为浓硫酸有吸水性,在陈红同学的实验中,浓硫酸增加的质量,不一定全部是吸收氨气的质量,也可能还有水的质量. |
相似问题
在电缆生产过程中会产生一定量的含铜废料.据报道 在通入空气并加热的条件下 铜与稀硫酸反应转化为硫酸铜
在电缆生产过程中会产生一定量的含铜废料.据报道,在通入空气并加热的条件下,铜与稀硫酸反应转化为硫酸铜.(1)请完成该反应的化学方程式2Cu+2H2SO4+O
长时间使用的热水壶底部有一层水垢 主要成分是CaCO3和Mg(OH)2.学校化学研究性学习小组同学通
长时间使用的热水壶底部有一层水垢,主要成分是CaCO3和Mg(OH)2.学校化学研究性学习小组同学通过实验想测定水垢中CaCO3的含量为多少.他们取200g水垢,
将65克不纯的锌片与足量的硫酸铜溶液充分反应后得到64克铜 则下列情况有可能是( )A.锌片中含有
将65克不纯的锌片与足量的硫酸铜溶液充分反应后得到64克铜,则下列情况有可能是( )A.锌片中含有铜和镁B.锌片中含有铁C.锌表面含有氧化锌D.锌片
用锌与硫酸溶液反应 五次实验结果记录如下:实验序号锌的质量/g硫酸溶液的质量/g在实验条件下氢气的体
用锌与硫酸溶液反应,五次实验结果记录如下:实验序号锌的质量 g硫酸溶液的质量 g在实验条件下氢气的体积 Ll6 52002 30213 02004 60319 52006 90426 0200
下列说法正确的是( )A.等质量的NaHCO3和MgCO3分别加入到足量稀盐酸中充分反应后 产生气
下列说法正确的是( )A.等质量的NaHCO3和MgCO3分别加入到足量稀盐酸中充分反应后,产生气体的质量相等B.等质量的足量的Fe和Al分别加入等质量的稀盐












