将2.34gNaCl固体溶于103.4g水中得到不饱和溶液 再向所得溶液中小心滴入200gAgNO3
| 将2.34gNaCl固体溶于103.4g水中得到不饱和溶液,再向所得溶液中小心滴入200gAgNO3溶液。实验过程中,生成的AgCl的质量与滴入的AgNO3溶液的质量关系如下图所示(提示:NaCl+AgNO3==AgCl↓+NaNO3 )。 |
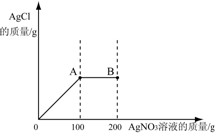 |
| (1)计算A点处生成NaNO3的质量? (2)计算B点溶液中AgNO3的溶质质量分数?(若最后结果不能整除,保留小数点后一位) |
参考解答
| (1)解:设A点处生成NaNO3的质量为x。 AgNO3+NaCl==AgCl↓+NaNO3 58.5 85 2.34g x 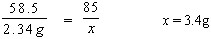 (2)设A点处反应AgNO3的质量为y,生成AgCl的质量为z。 AgNO3+NaCl=AgCl↓+NaNO3 170 58.5 143.5 y 2.34g z 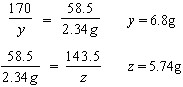 m(B点溶液)=2.34g+103.4g+200g-5.74g=300g B点溶液AgNO3的溶质质量分数= 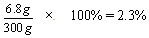 (其他合理解答参照给分) 答:A点处生成NaNO3的质量为3.4g,B点溶液AgNO3的溶质质量分数为2.3%。 |
相似问题
工业上用电解氯化镁的方法生产金属镁 Mg+Cl2==Mg+Cl2↑。问:电解950kg 氯化镁至多能
工业上用电解氯化镁的方法生产金属镁,Mg+Cl2==Mg+Cl2↑。问:电解950kg 氯化镁至多能生产多少千克金属?同时能得到多少千克氯气?
(1)实验室中要配制溶质质量分数为19.6%的稀硫酸200g 需要溶质质量分数为98%的浓硫酸的质量
(1)实验室中要配制溶质质量分数为19 6%的稀硫酸200g,需要溶质质量分数为98%的浓硫酸的质量是多少?(2)用上述配制的稀硫酸来测定某氢氧化钠溶液的质
CO是大气污染物之一。用氯化钯(PdCl2)可以测定空气中微量CO的含量 反应的化学方程式: PdC
CO是大气污染物之一。用氯化钯(PdCl2)可以测定空气中微量CO的含量,反应的化学方程式: PdCl2+CO+H2O= Pd↓+2HCl+CO2 测定某空气样品时,反应后得到
若将10g20%的NaOH溶液与10g20%的盐酸混合 下列叙述正确的是[ ]A 混合溶液的
若将10g20%的NaOH溶液与10g20%的盐酸混合,下列叙述正确的是[ ]A、混合溶液的pH=7B、溶液混合前后的温度不变C、混合溶液的质量为20gD、混合溶液中生成物
某学生在实验室称取m g CuO 用H2还原 反应一段时间后 停止加热 冷却 称量剩余固体 质量为n
某学生在实验室称取m g CuO,用H2还原,反应一段时间后,停止加热,冷却,称量剩余固体,质量为n g,则实验过程中消耗H2的质量为[ ]A B 大于 C 小于 D 无法计算












