(1)实验室中要配制溶质质量分数为19.6%的稀硫酸200g 需要溶质质量分数为98%的浓硫酸的质量
| (1)实验室中要配制溶质质量分数为19.6%的稀硫酸200g,需要溶质质量分数为98%的浓硫酸的质量是多少? (2)用上述配制的稀硫酸来测定某氢氧化钠溶液的质量分数。向80g滴有酚酞试液的该氢氧化钠溶液中逐滴滴加溶质质量分数为19.6%的稀硫酸,当红色恰好变成无色时,消耗稀硫酸的质量为50g。求氢氧化钠溶液中溶质的质量分数。 |
参考解答
| 解:(1)溶液在稀释前后溶液中溶质的质量分数不变,设需要溶质质量分数为98%的浓硫酸的质量是x,则:200g×19.6%=x×98% 解得:x=40g (2)在红色恰好变为无色时,氢氧化钠和硫酸恰好完全反应,此时消耗硫酸的质量为:50g×19.6%=9.8g 设氢氧化钠的质量为y H2SO4+2NaOH═=Na2SO4+2H2O 98 80 9.8g y 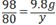 ;解得:y=8g ;解得:y=8g氢氧化钠溶液中溶质的质量分数为: 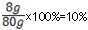 答:(1)需要溶质质量分数为98%的浓硫酸的质量是40g; (2)氢氧化钠溶液中溶质的质量分数为10%。 |
相似问题
CO是大气污染物之一。用氯化钯(PdCl2)可以测定空气中微量CO的含量 反应的化学方程式: PdC
CO是大气污染物之一。用氯化钯(PdCl2)可以测定空气中微量CO的含量,反应的化学方程式: PdCl2+CO+H2O= Pd↓+2HCl+CO2 测定某空气样品时,反应后得到
若将10g20%的NaOH溶液与10g20%的盐酸混合 下列叙述正确的是[ ]A 混合溶液的
若将10g20%的NaOH溶液与10g20%的盐酸混合,下列叙述正确的是[ ]A、混合溶液的pH=7B、溶液混合前后的温度不变C、混合溶液的质量为20gD、混合溶液中生成物
某学生在实验室称取m g CuO 用H2还原 反应一段时间后 停止加热 冷却 称量剩余固体 质量为n
某学生在实验室称取m g CuO,用H2还原,反应一段时间后,停止加热,冷却,称量剩余固体,质量为n g,则实验过程中消耗H2的质量为[ ]A B 大于 C 小于 D 无法计算
“5.12汶川大地震”发生后 药品是灾区最急需的救助物资之一。如图是一种救治伤员常用药品说明书的一部
“5 12汶川大地震”发生后,药品是灾区最急需的救助物资之一。如图是一种救治伤员常用药品说明书的一部分,请仔细阅读并回答有关问题。⑴不同规格的该药
把10g铁粉和铜粉的混合物放到盛有足量稀硫酸的烧杯中 充分反应后 烧杯中物质的总质量比反应前金属混合
把10g铁粉和铜粉的混合物放到盛有足量稀硫酸的烧杯中,充分反应后,烧杯中物质的总质量比反应前金属混合物与稀硫酸的总质量减少了0 1g,求原混合物中铁粉












