铜粉中常混有少量的氧化铜粉末 现要测量某铜粉样品中铜的质量分数 以下两组同学均取样品10g进行实验。
| 铜粉中常混有少量的氧化铜粉末,现要测量某铜粉样品中铜的质量分数,以下两组同学均取样品10g进行实验。 (Ⅰ)甲组同学准备用还原法还原氧化铜,实验室可用的还原剂有H2、CO、以及炭粉。 ①实验室中制取CO可用甲酸和浓硫酸加热反应制得,则制取CO气体可用到的仪器装置编号是(23)(从左图中选择,填写“a、b、c”编号)。图中编号“A”的仪器名称是(24)。 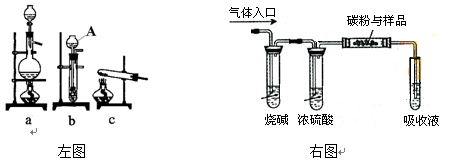 ②若利用气体进行还原,甲同学考虑使用H2,使用H2比使用CO的优点是 (25) 。如果反应前后样品质量减少0.08g,则样品中铜粉的质量分数是(26) 。 ③若利用右图装置进行碳还原氧化铜,利用吸收液吸收产生的CO2,在加热实验前,先通入N2赶尽装置内的剩余空气。吸收CO2溶液可以是(27)溶液。如果反应中只有CO2生成且完全被吸收,则得到CO2a mol时,样品中CuO的物质的量为(28) mol。 (Ⅱ)乙组同学采用稀硫酸反应的方法,实验的具体流程如下图所示: ④写出样品中加入稀硫酸发生的化学方程式 (29) ; ⑤该组所使用到的玻璃仪器有玻璃棒、烧杯以及(30) ,实验过程中使用玻璃棒的用途是搅拌和 (31) 。完成下列实验步骤,空白处实验操作的名称是 (32) 。 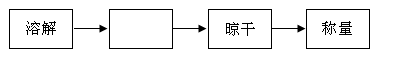 无论甲组还是乙组同学设计的实验,都利用了相同的化学原理,该化学原理是 (33)。 |
参考解答
(23)a (24)长颈漏斗 (25)CO有毒(或:使用氢气无需尾气吸收装置) (26)0.96(96%)(2分) (27)氢氧化钠 (28)2a (29)CuO+H2SO4→CuSO4+H2O (30)漏斗 (31)引流 (32)过滤 (33)质量守恒定律 |
| 分析:(Ⅰ) 可以用a装置制取一氧化碳; 氢气无毒,一氧化碳有毒,能够污染环境; 氢氧化钠能和二氧化碳反应生成碳酸钠和水; 氧化铜和稀硫酸反应能生成硫酸铜和水; 过滤时要用到漏斗,玻璃棒的作用有:搅拌、引流、转移物质; 在化学反应中遵循质量守恒定律. 解答:解: (Ⅰ)①实验室中制取CO可用甲酸和浓硫酸加热反应制得,则制取CO气体可用到的仪器装置编号是a.故填:a. 图中编号“A”的仪器名称是长颈漏斗.故填:长颈漏斗. ②使用H2比使用CO的优点是氢气无毒,使用氢气无需尾气吸收装置.故填:氢气无毒,使用氢气无需尾气吸收装置. 应前后样品质量减少0.08g,说明氧化铜中氧元素的质量是0.08g,根据氧化铜的化学式可知,氧化铜的质量是0.4g,铜的质量是9.6g,铜的质量分数为: 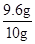 ×100%=96%.故填:96%. ×100%=96%.故填:96%.③吸收CO2溶液可以是氢氧化钠溶液.故填:氢氧化钠. 氧化铜和碳反应的化学方程式为:C+2CuO  2Cu+CO2↑,根据化学方程式可知,得到CO2a mol时,样品中CuO的物质的量为 2amol.故填:2a. 2Cu+CO2↑,根据化学方程式可知,得到CO2a mol时,样品中CuO的物质的量为 2amol.故填:2a.(Ⅱ)④样品中加入稀硫酸发生的化学方程式为:CuO+H2SO4═CuSO4+H2O. ⑤该组所使用到的玻璃仪器有玻璃棒、烧杯以及漏斗,实验过程中使用玻璃棒的用途是搅拌和引流.完成下列实验步骤,空白处实验操作的名称是过滤.故填:漏斗;引流;过滤. 无论甲组还是乙组同学设计的实验,都利用了相同的化学原理,该化学原理是质量守恒定律.故填质量守恒定律. |
相似问题
下列知识归纳 不完全正确的一组是A.化学反应中的能量变化①物质的缓慢氧化均放出热量②物质发生化学反应
下列知识归纳,不完全正确的一组是A.化学反应中的能量变化①物质的缓慢氧化均放出热量②物质发生化学反应的同时伴随着能量变化③在化学反应中只有燃烧才
某同学为制备二氧化碳 氢气和氧气 准备了下图所示的几种装置.(1)若用装置A制取氧气 在试管口放一团
某同学为制备二氧化碳、氢气和氧气,准备了下图所示的几种装置.(1)若用装置A制取氧气,在试管口放一团棉花,发生反应的化学方程式为:______.收集一
(1)根据实验提供的下列药品和仪器回答有关问题药品:石灰石 熟石灰 二氧化锰 氯酸钾 过氧化氢溶液
(1)根据实验提供的下列药品和仪器回答有关问题药品:石灰石、熟石灰、二氧化锰、氯酸钾、过氧化氢溶液、稀盐酸、稀硫酸.仪器如图1:①选择适当的药品
(7分)某化学兴趣小组设计出下列粗盐提纯的实验方案 请你一起来完成以下问题。(1) 操作①②③的名称
(7分)某化学兴趣小组设计出下列粗盐提纯的实验方案,请你一起来完成以下问题。(1) 操作①②③的名称依次是 ▲、 ▲、 ▲;若在操作②结束后发现溶
炭雕(见右图)是一种集观赏与空气净化为一体的产品。这种产品可对车内及室内空气中的一氧化碳 甲醛等有害
炭雕(见右图)是一种集观赏与空气净化为一体的产品。这种产品可对车内及室内空气中的一氧化碳、甲醛等有害气体进行有效吸附。某课外小组想对炭雕产品进












