溶液的浓度有哪些常用的表示方法?试比较各种浓度表示方法在实际使用中的优缺点。对于稀的水溶液 试推导其
溶液的浓度有哪些常用的表示方法?试比较各种浓度表示方法在实际使用中的优缺点。对于稀的水溶液,试推导其质量摩尔浓度和溶质的摩尔分数的关系式。
请帮忙给出正确答案和分析,谢谢!
参考解答
正确答案:常用的溶液浓度表示方法有如下4种: (1)物质的量浓度溶液中所含溶质B的物质的量除以溶液的体积称为B的物质的量浓度可简称为浓度用符号c表示即 cB=nB/V 在温度不变的情况下配制溶液或按要求转移溶液时使用物质的量浓度十分方便但是物质的量浓度会受到温度变化的影响。 (2)质量摩尔浓度溶液中所含溶质B的物质的量nB除以溶剂的质量mA称为B的质量摩尔浓度用符号bB或mB表示即 bB=nB/mA 质量摩尔浓度最大的优点是不会受到温度变化的影响。但使用移液管和滴定管时必须知道溶液的密度才能计算出所转移溶液中溶质的物质的量。 (3)质量分数物质B的质量mB与混合物的质量m之比称为物质B的质量分数。质量分数用符号w表示即 wB=mB/m 当人们更注重溶液中溶质的质量而不是其物质的量时质量分数这种溶液浓度表示方法就显得十分有意义;但是当人们注重的是溶质的物质的量时质量分数应用起来就不十分方便。 对于溶液而言mB代表溶质B的质量m代表溶液的质量。 (4)摩尔分数溶液中溶质的物质的量n质与溶液的总物质的量n液之比叫做溶质的摩尔分数用符号x质表示即 x质=n质/n液 或 x质=n质/(n质+n剂) 摩尔分数既不体现溶液的质量又不体现溶液的体积不是实验中常用的浓度表示方法。这种浓度的意义在于可以很好地从溶质和溶剂的物质的量的关系方面表示溶液的组成。 对于稀溶液有x剂》x质所以x剂+x质=x剂所以 x质=n质/(n质+n剂)≈n质/n液 对于水溶液当n剂=1000g/18g.mol-1=55.56mol时其所对应的n质正是1000g溶液中所含的溶质的物质的量。所以n质的数值上等于溶质的质量摩尔浓度b质于是有关系式 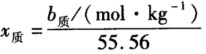
常用的溶液浓度表示方法有如下4种:(1)物质的量浓度溶液中所含溶质B的物质的量,除以溶液的体积,称为B的物质的量浓度,可简称为浓度,用符号c表示,即cB=nB/V在温度不变的情况下,配制溶液或按要求转移溶液时,使用物质的量浓度十分方便,但是物质的量浓度会受到温度变化的影响。(2)质量摩尔浓度溶液中所含溶质B的物质的量nB,除以溶剂的质量mA,称为B的质量摩尔浓度,用符号bB或mB表示,即bB=nB/mA质量摩尔浓度最大的优点是不会受到温度变化的影响。但使用移液管和滴定管时,必须知道溶液的密度才能计算出所转移溶液中溶质的物质的量。(3)质量分数物质B的质量mB与混合物的质量m之比称为物质B的质量分数。质量分数用符号w表示,即wB=mB/m当人们更注重溶液中溶质的质量而不是其物质的量时,质量分数这种溶液浓度表示方法就显得十分有意义;但是当人们注重的是溶质的物质的量时,质量分数应用起来就不十分方便。对于溶液而言,mB代表溶质B的质量,m代表溶液的质量。(4)摩尔分数溶液中溶质的物质的量n质与溶液的总物质的量n液之比叫做溶质的摩尔分数,用符号x质表示,即x质=n质/n液或x质=n质/(n质+n剂)摩尔分数既不体现溶液的质量,又不体现溶液的体积,不是实验中常用的浓度表示方法。这种浓度的意义在于可以很好地从溶质和溶剂的物质的量的关系方面表示溶液的组成。对于稀溶液有x剂》x质,所以x剂+x质=x剂,所以x质=n质/(n质+n剂)≈n质/n液对于水溶液,当n剂=1000g/18g.mol-1=55.56mol时,其所对应的n质正是1000g溶液中所含的溶质的物质的量。所以n质的数值上等于溶质的质量摩尔浓度b质,于是有关系式
相似问题
利用下列级数求下列级数的收敛域 以及它们在收敛域内的和函数:求下列级数的收敛域 以及它们在收敛域内的
利用下列级数求下列级数的收敛域,以及它们在收敛域内的和函数:求下列级数的收敛域,以及它们在收敛域内的和函数: 请帮忙给出正确答案和分析,谢谢!
求方程xy〞一yˊ=x2的通解.请帮忙给出正确答案和分析 谢谢!
求方程xy〞一yˊ=x2的通解.请帮忙给出正确答案和分析,谢谢!
判别下列级数是绝对收敛 条件收敛 还是发散: 此题为判断题(对 错)。请帮忙给出正确答案和分析 谢谢
判别下列级数是绝对收敛、条件收敛,还是发散: 此题为判断题(对,错)。请帮忙给出正确答案和分析,谢谢!
求y〞+4y=2x+sin 2x的通解.请帮忙给出正确答案和分析 谢谢!
求y〞+4y=2x+sin 2x的通解.请帮忙给出正确答案和分析,谢谢!
设A为3阶矩阵 P为3阶可逆矩阵 且P-1AP=若P=(α1 α2 α3) Q=(α1+α2 α2
设A为3阶矩阵,P为3阶可逆矩阵,且P-1AP=若P=(α1,α2,α3),Q=(α1+α2,α2,α3),则Q-1AQ=A.B.C.D.请帮忙给出正确答案和分析,谢谢!












