在下列两个反应中被氧化的氯元素与被还原的氯元素的质量之比各为多少?(1)2Cl2+2Ca(OH)2=
| 在下列两个反应中被氧化的氯元素与被还原的氯元素的质量之比各为多少? (1)2Cl2+2Ca(OH)2====CaCl2+Ca(ClO)2+2H2O (2)3Cl2+6KOH 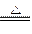 5KCl+KClO3+3H2O 5KCl+KClO3+3H2O |
参考解答
| (1)1∶1 (2)1∶5 |
| (1)(2)两个反应均是歧化反应,(1)中2个Cl2分子中的4个Cl原子有2个失电子,有2个得电子;(2)中3个Cl2分子中的6个Cl原子中有1个失电子生成KClO3,有5个得电子。失电子被氧化,得电子被还原。 |
相似问题
黑火药发生反应2KNO3+S+3C====K2S+N2↑+3CO2↑中 被还原的元素是( )A.
黑火药发生反应2KNO3+S+3C====K2S+N2↑+3CO2↑中,被还原的元素是()A.氮和氧B.碳C.氮和硫D.氮和碳
将铁粉加入到一定量的硝酸银 硝酸铜及硝酸锌的混合溶液中 待充分反应后过滤 在滤渣中加入稀盐酸 没有气
将铁粉加入到一定量的硝酸银、硝酸铜及硝酸锌的混合溶液中,待充分反应后过滤,在滤渣中加入稀盐酸,没有气体产生,则在滤液中( )A.只有硝酸锌和水B.
下列说法正确的是[ ]A.置换反应一定属于氧化还原反应B.分解反应均不属于氧化还原反应C.复
下列说法正确的是[ ]A.置换反应一定属于氧化还原反应B.分解反应均不属于氧化还原反应C.复分解反应有的属于氧化还原反应D.化合反应一定属于氧化还原反应
下列氧化还原反应的方程式配平正确的是( )A.Fe3++ S2-====Fe2++SB.Fe3+
下列氧化还原反应的方程式配平正确的是()A.Fe3++ S2-====Fe2++SB.Fe3++Fe= "===2 " Fe2+C.Fe2++Cl2====Fe3++2 Cl-D.2 Fe3++2I-= "===2 " Fe2++I2
下列说法不正确的是[ ]A.凡有单质参加的化合反应都是氧化还原反应 B.所有的复分解反应都是
下列说法不正确的是[ ]A.凡有单质参加的化合反应都是氧化还原反应 B.所有的复分解反应都是非氧化还原反应 C.盐酸在参加的反应中只能作氧化剂D.金












