(14分)黄铜矿是工业炼铜的主要原料 其主要成分为CuFeS2 现有一种天然黄铜矿(含少量脉石SiO
(14分)黄铜矿是工业炼铜的主要原料,其主要成分为CuFeS2,现有一种天然黄铜矿(含少量脉石SiO2),为了测定该黄铜矿的纯度,某同学设计了如下实验: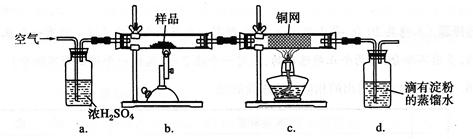  现称取研细的黄铜矿样品1.150 g,在空气存在下进行煅烧,生成Cu、Fe2O3、FeO和SO2气体,实验后取d中溶液的1/10置于锥形瓶中,用0.05000 mol·L-1标准碘溶液进行滴定,初读数为0.10 mL,末读数如右图所示。 (1)冶炼铜的反应为8CuFeS2+ 21O2 高温8Cu + 4FeO + 2Fe2O3+ 16SO2,若CuFeS2中Fe的化合价为+2,反应中被还原的元素是 (填元素符号)。 (2)装置a的作用是 。
(4)滴定时,标准碘溶液所耗体积为 mL。用化学方程式表示滴定的原理: 。 (5)通过计算可知,该黄铜矿的纯度为 。 |
参考解答
| (1)Cu、O (2分); (2)BD (2分);(3)将系统装置中SO2全部排入d中充分吸收(2分) (4)20.00 (2分);I2+ SO2+ 2H2O=H2SO4+ 2HI(3分) (5)80.00%(3分) |
试题分析:(1)若CuFeS2中Fe的化合价为+2,则铜元素和硫元素的化合价分别为+2价和-2价。根据化学方程式可知,反应后铜元素化合价降低,氧元素化合价也降低,硫元素化合价升高,铁元素化合价部分升高,因此反应中被还原的元素是Cu和O。 (2)由于空气中含有水蒸气,因此浓硫酸的作用是干燥空气。另外通过观察a装置中气泡可以控制气体的流速以便于控制反应,故答案为BD。 (3)由于装置还含有未被吸收的SO2,因此继续投入空气的目的是将系统装置中SO2全部排入d中充分吸收。 (4)根据滴定管的液面可知,读数是20.10ml,因此实际消耗标准液的体积为20.10ml-0.10ml=20.00ml。二氧化硫具有还原性,能被碘氧化生成 硫酸,反应的离子方程式为I2+ SO2+ 2H2O=H2SO4+ 2HI。 (5)消耗标准碘的物质的量=0.05000 mol·L-1×0.02000L=0.001000mol,所以根据方程式可知参加反应的二氧化硫的物质的量是0.001000mol,则样品产生的二氧化硫的物质的量是0.001000mol×10=0. 01000mol。因此根据方程式可知CuFeS2的物质的量是0.005ml,质量是0.005ml×184g/mol=0.92g,因此该黄铜矿的纯度为 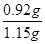 ×100%=80.00% ×100%=80.00% |
相似问题
Na2FeO4是一种高效多功能水处理剂 一种制备Na2FeO4的方法可用化学方程式表示如下:2FeS
Na2FeO4是一种高效多功能水处理剂,一种制备Na2FeO4的方法可用化学方程式表示如下:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2+O2↑。下列对此反应的说法中,不
某金属单质能与足量浓硝酸反应 放出NO2气体 若参加反应的金属单质与硝酸的物质的量之比为1:a 则该
某金属单质能与足量浓硝酸反应,放出NO2气体,若参加反应的金属单质与硝酸的物质的量之比为1:a,则该金属元素在反应后生成的硝酸盐中的化合价是A.+2aB
铜是生物体必需的微量元素 也是人类最早使用的金属之一。铜的生产和使用对国计民生各个方面都产生了深远的
铜是生物体必需的微量元素,也是人类最早使用的金属之一。铜的生产和使用对国计民生各个方面都产生了深远的影响。(1)写出铜与稀硝酸反应的化学方程式:
向一定量的Fe FeO和Fe2O3的混合物中加入120 mL 4 mol·L-1的稀硝酸 恰好使混合
向一定量的Fe、FeO和Fe2O3的混合物中加入120 mL 4 mol·L-1的稀硝酸,恰好使混合物完全溶解,放出1 344 L NO(标准状况),往所得溶液中加入KSCN溶液
某元素在化学反应中 由化合态变为游离态 则该元素[ ]A.一定被氧化 B.一定被还原 C
某元素在化学反应中,由化合态变为游离态,则该元素[ ]A.一定被氧化 B.一定被还原 C.可能被氧化,也可能被还原 D.化合价降低为0












