高锰酸钾是一种典型的强氧化剂。完成下列填空:Ⅰ.在用KMnO4酸性溶液处理Cu2S和CuS的混合物时
| 高锰酸钾是一种典型的强氧化剂。 完成下列填空: Ⅰ.在用KMnO4酸性溶液处理Cu2S和CuS的混合物时,发生的反应如下: ① MnO4-+ Cu2S + H+→ Cu2+ + SO2↑ + Mn2+ + H2O(未配平) ② MnO4-+ CuS + H+ → Cu2+ + SO2↑ + Mn2++ H2O(未配平) (1)下列关于反应①的说法中错误的是 (选填编号)。 a.被氧化的元素是Cu和S b.氧化剂与还原剂的物质的量之比为8:5 c.生成2.24 L(标况下) SO2,转移电子的物质的量是0.8 mol d.还原性的强弱关系是: Mn2+> Cu2S (2)标出反应②中电子转移的方向和数目: MnO4-+ CuS Ⅱ.在稀硫酸中,MnO4-和H2O2也能发生氧化还原反应 氧化反应:H2O2-2e → 2H+ + O2↑ 还原反应:MnO4- + 5e + 8H+ → Mn2+ + 4H2O (3)反应中若有0.5 mol H2O2参加此反应,转移电子的个数为 。由上述反应得出的物质氧化性强弱的结论是 >___________(填写化学式)。 (4)已知:2KMnO4+ 7H2O2+3H2SO4→ K2SO4+2MnSO4 +6O2↑+10H2O,则被1mol KMnO4氧化的H2O2是 mol。 |
参考解答
| (1)d (2分) (2) 6MnO4-+ 5CuS (2分,系数1分,电子转移的数目和方向都对1分) (3)6.02×1023 (1分); KMnO4> H2O2(或O2) (1分) (4)2.5 (2分) |
试题分析::(1)a.反应中铜元素化合价从+1价升高到+2价,硫元素化合价从-2价升高到+4价,化合价升高的元素被氧化,所以被氧化的元素有S、Cu,故a正确; b.锰元素化合价降低,从+7价降低为+2价,Cu2S元素化合价都升高做还原剂,1molMnO4-得到5mol电子,反应中铜元素化合价从+1价升高到+2价,硫元素化合价从-2价升高到+4价,1molCu2S失去8mol电子,则氧化剂与还原剂的物质的量之比为8:5,故b正确; c.生成2.24LL(标况下)SO2时,物质的量为0.1mol;反应的Cu2S物质的量为0.1mol,反应中转移电子的物质的量是: 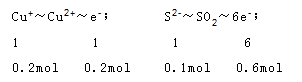 所以电子转移共0.8mol,故c正确; d.氧化还原反应中还原剂的还原性大于还原产物的还原性,则还原性的强弱关系是:Mn2+<Cu2S,故d错误.故选d. (2)反应②中Mn元素化合价降低,从+7价降低为+2价,1molMnO4-得到5mol电子,CuS中硫元素化合价从-2价升高到+4价,1molCuS失去6mol电子,则二者物质的量之比为6:5,转移电子数目为5×6=30,可表示为 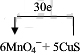 ,故答案为: ,故答案为: ; ;(3)由H2O2-2e→2H++O2↑可知,反应中若有0.5mol H2O2参加此反应,转移电子的个数为0.5×2×NA=NA,在反应中MnO4-为氧化剂,H2O2为还原剂,则氧化性MnO4->H2O2,故答案为:NA;MnO4-;H2O2; (4)反应2KMnO4+7H2O2+3H2SO4→K2SO4+2MnSO4+6O2↑+10H2O中,2molKMnO4可氧化5molH2O2,生成的6molO2中,有5mol为H2O2被氧化生成,有1mol为H2O2自身发生氧化还原反应生成,则1mol KMnO4氧化的H2O2是2.5mol,故答案为:2.5。 |
相似问题
Cu2S与一定浓度的HNO3反应 生成Cu(NO3)2 CuSO4 NO2 NO和H2O。当产物中
Cu2S与一定浓度的HNO3反应,生成Cu(NO3)2、CuSO4、NO2、NO和H2O。当产物中n(NO2)∶n(NO)=1∶1时,下列说法正确的是()A.产物中n[Cu(NO3)2]∶n[CuSO4
实验室里迅速制备少量氯气可利用以下反应: KMnO4+ HCl KCl +
实验室里迅速制备少量氯气可利用以下反应:KMnO4+HCl KCl + MnCl2 +Cl2↑ + H2O (1)请配平上述化学方程式,并在上面用“双线桥法” 标明电子转
由一种阳离子与两种酸根离子组成的盐称为混盐。混盐CaOC12在酸性条件下可以产生C12
由一种阳离子与两种酸根离子组成的盐称为混盐。混盐CaOC1­2在酸性条件下可以产生C12,下列关于混盐CaOC12的有关判断不正确的是A.该混盐与硫酸反应产
锰酸钾可用于油脂 纤维 皮革的漂白等 其可由KOH KClO3和MnO2经共熔制备 反应原理为6KO
锰酸钾可用于油脂、纤维、皮革的漂白等,其可由KOH、KClO3和MnO2经共熔制备,反应原理为6KOH+KClO3+3MnO2KCl+3K2MnO4+3H2O。下列有关说法中正确的是
火药是中国的“四大发明”之一 永远值得炎黄子孙骄傲 也永远会激励着我们去奋 发图强。黑火药在发生爆炸
火药是中国的“四大发明”之一,永远值得炎黄子孙骄傲,也永远会激励着我们去奋 发图强。黑火药在发生爆炸时,发生如下的反应:2KNO3+3C+S===K2S+N2↑+












