(13分)过氧化钠(化学式为NaNa2O2)可用在呼吸面具中作为氧气来源。Na2O2能跟CO2反应
| (13分)过氧化钠(化学式为NaNa2O2)可用在呼吸面具中作为氧气来源。Na2O2能跟CO2反应生成O2和另一种固体化合物(用X表示);它也能跟H2O反应生成O2,化学方程式为:2Na2O2+2H2O = 4NaOH+O2↑。以下是某兴趣小组进行的探究活动。 (1)利用如下图所示实验装置制取氧气,请回答有关问题。 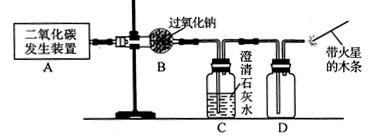 ①实验室制取CO2的化学方程式为 。 ②表明CO2未被Na2O2完全吸收的实验现象为 。 ③O2可采用D装置收集,并用带火星的木条检验,这是利用了O2的 性质。 ④若A装置产生的CO2中混有水蒸气,要检验干燥的CO2能否与Na2O2反应生成O2,以上实验装置应如何改进 (2)为探究X是哪种物质及其有关性质,同学们进行了如下分析和实验。 ①有同学猜想X可能是酸、碱或盐中的一种。通过对物质组成的分析,大家一致认为X肯定不是酸和碱,理由是 。 ②同学们通过讨论和实验证明了X是Na2CO3。以下是他们设计的有关Na2CO3性质的探究实验,将下表填写完整。
|
参考解答
| (1)①CaCO3+2HCl==CaCl2+H2O+CO2↑ ②澄清石灰水变浑浊 ③氧气密度比空气的大,氧气有助燃性。 ④在A、B装置之间增加气体干燥装置 (2)①Na2O2和CO2都不含氢元素,根据质量守恒定律,二者反应后不可能生成含氢 元素的酸或碱(1分) ②
2Na2O2+2H2O=4NaOH+O2↑ 156 160 32 7.8g y x X=1.6g Y=8g 氢氧化钠溶液中溶质的质量分数为: 8g/40g×100%=20% 答:略。 |
试题分析:(1)①实验室用大理石和稀盐酸制备CO2,其反应为CaCO3+2HCl==CaCl2+H2O+CO2↑ ②装置C中的澄清石灰水就是检验CO2是否反应完全,如果CO2没有反应完全,则C中的澄清石灰水变浑浊③D装置长进短处是向上排空气的方法,因为氧气的密度比空气大,所以采用向上排空气法收集气体,氧气能使带火星的木条复燃,是因为氧气具有助燃性。④因为制出的CO2带有水,所以要在A、B之间加一个干燥装置 (2)①因为反应物是Na2O2和CO2,因此在产物中不可能有H元素出现,而酸或碱中都含有H元素,所以X不可能是酸或碱。②根据反应方程式可知,是盐酸与碳酸钠反应,盐酸与碳酸钠反应的现象是产生气泡。根据碳酸钠的性质可知,碳酸钠与钙盐或钡盐反应会产生白色沉淀。 (3)解:设生成氧气的质量为x,生成氢氧化钠的质量为y。 2Na2O2+2H2O=4NaOH+O2↑ 156 160 32 7.8g y x X=1.6g Y=8g 氢氧化钠溶液中溶质的质量分数为: 8g/40g×100%=20% 答:氢氧化钠溶液中溶质的质量分数为20%。2O2的性质、Na2CO3的性质,溶液质量分数的计算 点评:这是一道综合性强的实验习题,既有实验装置的分析,又有物质性质的检验,还有溶液质量分数的计算,要想能准确解答这类习题,首先要会分析各仪器的作用,然后掌握各种物质的性质。 |
相似问题
金属钠分别与下列溶液反应 既有气体又有沉淀产生的是( )A.NaHCO3B.BaCl2C.Na
金属钠分别与下列溶液反应,既有气体又有沉淀产生的是( )A.NaHCO3B.BaCl2C.Na2CO3D.CuSO4
用一小粒钠投入水中 实验操作和过程中不可能感知或观察到的现象是A.钠的熔点低B.钠呈银白色 硬度小C
用一小粒钠投入水中,实验操作和过程中不可能感知或观察到的现象是A.钠的熔点低B.钠呈银白色、硬度小C.钠有延展性,导电性好D.钠具有强还原性
下列有关Na2CO3和NaHCO3性质的比较中 正确的是A.固体的热稳定性:Na2 CO3>NaHC
下列有关Na2CO3和NaHCO3性质的比较中,正确的是A.固体的热稳定性:Na2 CO3>NaHCO3B.与稀盐酸反应放出气体的快慢:Na2CO3>NaHCO3C.106gNa2CO3和84gNaH
某校化学研究性学习小组设计如下实验方案 测定放置已久的小苏打样品中纯碱的质量分数。(1)方案一:称取
某校化学研究性学习小组设计如下实验方案,测定放置已久的小苏打样品中纯碱的质量分数。(1)方案一:称取一定质量的样品,置于坩埚中加热至恒重后,冷却
在“绿色化学实验进课堂”活动中 某同学为“氯气与金属钠反应”设计了下图装置与操作以替代相关的课本实验
在“绿色化学实验进课堂”活动中,某同学为“氯气与金属钠反应”设计了下图装置与操作以替代相关的课本实验。将一根玻璃管与氯气发生器相连,玻璃管内放












