已知酸性高锰酸钾溶液可以将FeSO4氧化 方程式为2KMnO4+10FeSO4+ 8H2SO4=K2
已知酸性高锰酸钾溶液可以将FeSO4氧化,方程式为2KMnO4+10FeSO4+ 8H2SO4=K2SO4+2MnSO4+5Fe2(SO4)3+8H2O,现将一定量的硫酸酸化的高锰酸钾溶液与硫酸亚铁溶液混合,充分反应后再向所得溶液中加入KI溶液,混合溶液中铁离子的物质的量随加入的KI的物质的量的变化关系如下图所示。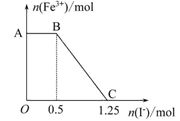 则下列有关说法不正确的是( )
|
参考解答
| D |
| 加入KI溶液后,AB段,Fe3+的物质的量不变,说明高锰酸钾溶液与硫酸亚铁溶液反应后高锰酸钾过量,根据电子守恒可知,过量的n(KMnO4)为0.5 mol÷5='0.1' mol。继续加入KI溶液,Fe3+的物质的量减少,发生反应2Fe3++2I-=2Fe2++I2,反应的n(Fe3+)='0.75' mol,所以生成0.75 mol Fe3+消耗的n(KMnO4)为0.75 mol÷5='0.15' mol,则开始加入的高锰酸钾的物质的量为0.25 mol。C点以后的溶液中不再含有Fe3+,加入少量KSCN溶液,溶液颜色不变 |
相似问题
下列反应离子方程式正确的是 A.过量石灰水与碳酸氢钙反应:Ca2++2HCO3-+2OH-=CaCO
下列反应离子方程式正确的是 A.过量石灰水与碳酸氢钙反应:Ca2++2HCO3-+2OH-=CaCO3↓+CO32-+2H2OB.FeSO4酸性溶液暴露在空气中:4Fe2++O2+4H
下列方程式不正确的是A.用稀H2SO4吸收氨气:NH3+H+=NH4+B.少量的CO2通入NaOH溶
下列方程式不正确的是A.用稀H2SO4吸收氨气:NH3+H+=NH4+B.少量的CO2通入NaOH溶液中:CO2+2OH-=CO32-+H2OC.铜溶解于氯化铁溶液中:2Fe3++Cu=2Fe
铬(Cr)属于重金属元素 含铬的废水和废渣排放必须经过处理达到有关的安全标准。(1)铬原子核中质子数
铬(Cr)属于重金属元素,含铬的废水和废渣排放必须经过处理达到有关的安全标准。(1)铬原子核中质子数为24,铬位于周期表中第______周期。(2)铬元素
已知 0.4 mol 液态肼和足量H2O2反应生成氮气和水蒸气时放出256.64 kJ的热量。(1)
已知 0 4 mol 液态肼和足量H2O2反应生成氮气和水蒸气时放出256 64 kJ的热量。(1)写出肼和H2O2反应的热化学方程式:。(2)已知H2O(l)=H2O(g) ΔH="+44"
下列离子方程式中正确的是A.用FeCl3溶液腐蚀印刷电路板:Fe3++Cu=Fe2++Cu2+B.等
下列离子方程式中正确的是A.用FeCl3溶液腐蚀印刷电路板:Fe3++Cu=Fe2++Cu2+B.等体积、等物质的量浓度的NaHCO3溶液和Ca(OH)2溶液混合:HCO3-+Ca2++OH-=












