(1)已知:N2(g)+O2(g)=2NO(g);△H= +180.5kJ/mol4NH3(g)+5
| (1)已知:N2(g)+O2(g)=2NO(g);△H= +180.5kJ/mol 4NH3(g)+5O2(g)=4NO(g)+6H2O(g);△H=-905kJ/mol 2H2(g)+O2(g)=2H2O(g);△H=-483.6kJ/mol 则N2(g)+3H2(g)=2NH3(g)的△H= 。 (2)工业合成氨的反应为N2(g)+3H2(g)  2NH3(g)。在一定温度下,将一定量的N2和H2通入固定体积为1L的密闭容器中达到平衡后,改变下列条件,能使平衡向正反应方向移动的是 。 2NH3(g)。在一定温度下,将一定量的N2和H2通入固定体积为1L的密闭容器中达到平衡后,改变下列条件,能使平衡向正反应方向移动的是 。①增大压强 ②通入He ③使用催化剂 ④降低温度 (3)工业合成氨的反应为N2(g)+3H2(g)  2NH3(g)。设在容积为2.0L的密闭容器中充入0.60molN2(g)和1.60molH2(g),反应在一定条件下达到平衡时,NH3的物质的量分数(NH3的物质的量与反应体系中总的物质的量之比)为 2NH3(g)。设在容积为2.0L的密闭容器中充入0.60molN2(g)和1.60molH2(g),反应在一定条件下达到平衡时,NH3的物质的量分数(NH3的物质的量与反应体系中总的物质的量之比)为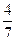 。计算该条件下达到平衡时N2转化率为 ; 。计算该条件下达到平衡时N2转化率为 ;(4)合成氨的原料氢气是一种新型的绿色能源,具有广阔的发展前景。现用氢氧燃料电池进行右图所示实验:(其中c、d均为碳棒,NaCl溶液的体积为500ml) 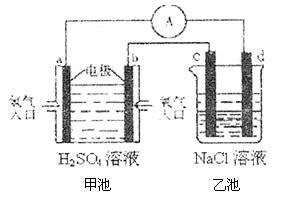 ①b极为 极,电极反应式 ; c极为 极,电极反应式  ②右图装置中,当b极上消耗的O2在标准状况下的体积为280ml时,则乙池溶液的PH为 (假设反应前后溶液体积不变,且NaCl溶液足量) |
参考解答
| (1)△H=-92.4kJ/mol (2分) (2)① ④ (2分) (3)66.67% 或2/3 (2分) (4)①正极,O2+4H++4e-=2H2O;阳极,2Cl--2e-=Cl2↑(每空2分,共8分) ② 13(2分) |
| 略 |
相似问题
目前工业上有一种方法是用CO2来生产燃料甲醇。CO2(g)+3H2(g)CH3OH(g)+H2O(g
目前工业上有一种方法是用CO2来生产燃料甲醇。CO2(g)+3H2(g)CH3OH(g)+H2O(g)ΔH=-49 0kJ mol,为探究反应原理,现进行如下实验:在体积为1 L的密闭
一定温度下 反应N2(g)+3H 2(g) 2NH3(g)达到化学平衡状态的标志是A.混合气体的总质
一定温度下,反应N2(g)+3H 2(g) 2NH3(g)达到化学平衡状态的标志是A.混合气体的总质量不再改变B.混合气体的平均相对分子质量不再改变C.N2与H2的物质
已建立化学平衡的某可逆反应 当改变某反应条件使平衡向正反应方向移动时 下列有关叙述正确的是A.正反应
已建立化学平衡的某可逆反应,当改变某反应条件使平衡向正反应方向移动时,下列有关叙述正确的是A.正反应速率一定增大B.生成物的质量分数一定增大C.逆
在体积为IL的密闭容器中 充入1mol CO2和3mol H2 —定条件下发生反应:测得C02(g)
在体积为IL的密闭容器中,充入1mol CO2和3mol H2,—定条件下发生反应:测得C02(g)和CH30H(g)的浓度随时间变化如图所示,则下列说法正确的是A 反应进
向一个体积可变的密闭容器中充入4mol A 1mol B 发生如下反应:4A(g)+B(s)3C
向一个体积可变的密闭容器中充入4mol A、1mol B,发生如下反应:4A(g)+B(s)3C(s)+4D(g)。在高温下达到平衡,测得混合气体中D的浓度为0 3mol·L-












