在溶液中 反应A+2BC分别在三种不同实验条件下进行 它们的起始浓度均为c(A)='0.100' m
在溶液中,反应A+2B C分别在三种不同实验条件下进行,它们的起始浓度均为c(A)="0.100" mol·L-1c(B)="0.200" mol·L-1 c(C)="0" mol·L-1。反应物A的浓度随时间的变化如右图所示。 C分别在三种不同实验条件下进行,它们的起始浓度均为c(A)="0.100" mol·L-1c(B)="0.200" mol·L-1 c(C)="0" mol·L-1。反应物A的浓度随时间的变化如右图所示。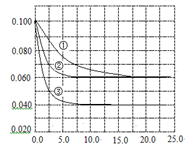 A.若反应①、②的平衡常数分别为K1、K2,则K1< K2 B.反应A+2B  C的△H>0 C的△H>0C.实验②平衡时B的转化率为60% D.减小反应③的压强,可以使平衡时c(A)="0.060" mol·L-1 |
参考解答
| B |
| 首先声明一下:本题有很大的漏洞: ①题干不完整:应补充一句“下列说法正确的是:” ②原题所给答案是错误的,应选B而不是D。 本题重点考查的知识点: “影响化学平衡移动的外界因素:温度、浓度、压强、催化剂”、“影响化学平衡常数的因素——温度”以及“有关化学平衡的简单计算:如化学反应速率、转化率” 解析: 首先:注意分析题干中的关键词:“在溶液中”——所以改变压强对该反应几乎无任何影响,因为压强只对有气体参加的化学反应有影响;“分别在三种不同的条件下”——曲线①②③的条件各不相同。由于影响平衡的外因有温度、浓度、压强、催化剂,但题中起始浓度均已相同,所曲线①②③改变的条件只可能是温度和催化剂。 其次:分析图像。要抓住图像中的关键点——起点、拐点来解题 A项:①②相对比——达到平衡的时间缩短,但平衡时A的浓度不变,所以②相对①而言加了催化剂。由于平衡常数只受温度影响,所以K1=K2 B项:①③相比——到达平衡的时间缩短,但平衡时A的浓度变化了,所以③相对①而言升高了温度。由图知,升高温度,A的浓度减小,所以平衡正向移动,故正反应为吸热反应, △H>0 C项:由曲线②可知,A的平衡浓度变化量为0.04mol/L,得出B的平衡浓度变化量为0.08mol/L,所以平衡时B转化率为0.08/0.2=40% D项:在溶液中的反应,改变压强对平衡无影响 |
相似问题
(14分)能源开发 环境保护 资源利用等是当今社会的热门话题。请根据所学化学知识回答下列问题:(1)
(14分)能源开发、环境保护、资源利用等是当今社会的热门话题。请根据所学化学知识回答下列问题:(1)汽车上安装催化转化器,可使汽车尾气中的主要污染
( 14分)在T℃条件下 向1L固定体积的密闭容器M中加入2 mol X和1 mol Y 发生如下反
( 14分)在T℃条件下,向1L固定体积的密闭容器M中加入2 mol X和1 mol Y,发生如下反应:2X(g) + Y(g)a Z(g) + W(g) △H = -Q kJ
下列能用勒夏特列原理解释的是A.Fe(SCN)3溶液中加入固体KSCN后颜色变深B.棕红色NO2加压
下列能用勒夏特列原理解释的是A.Fe(SCN)3溶液中加入固体KSCN后颜色变深B.棕红色NO2加压后颜色先变深后变浅C.SO2催化氧化成SO3的反应,往往需要使用催
(共10分)在一定条件下 将3molA 和1mol B 两种气体混合于固定容积为2L的密闭容器中 发
(共10分)在一定条件下,将3molA 和1mol B 两种气体混合于固定容积为2L的密闭容器中,发生如下反应:3A(g)+B(g)xC(g)+ 2D(g)。2min末该反应
(共8分)(1)(3分)有反应:2NO2N2O4 △H
(共8分)(1)(3分)有反应:2NO2N2O4△H<0,根据图像判断后填空:Vt1 t2 t3 t4 t5 t6 tt1至t3采取的措施是_____________;t4至t5采取的措施是__












