用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反
| 用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题: (1)烧杯间填满碎纸条的作用是______. (2)用浓硫酸代替盐酸溶液进行上述实验,测得的中和热的数值会______;(填“偏大”、“偏小”、“无影响”). (3)若某同学利用上述装置做实验,有些操作不规范,造成测得中和热的数值偏低,请你分析可能的原因是______ A.测量盐酸的温度后,温度计没有用水冲洗干净 B.把量筒中的氢氧化钠溶液倒入小烧杯时动作迟缓 C.做本实验的当天室温较高 D.将50mL0.55mol/L氢氧化钠溶液取成了50mL0.55mol/L的氨水 E.在量取盐酸时仰视计数 F.大烧杯的盖板中间小孔太大. 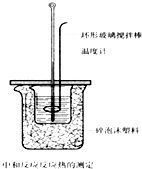 |
参考解答
| (1)根据量热计的构造和实验的成败关键来判断该装置的大小烧杯间填满碎纸条的作用是保温、隔热,防止热量散失,故答案为:保温、隔热,防止热量散失; (2)浓硫酸在稀释过程中会放出大量的热量,导致中和热的数值会偏高,故答案为:偏大; (3)A.测量盐酸的温度后,温度计没有用水冲洗干净,在测碱的温度时,会发生酸和碱的中和,温度计示数变化值减小,所以导致实验测得中和热的数值偏小,故A正确; B、把量筒中的氢氧化钠溶液倒入小烧杯时动作迟缓,会导致一部分能量的散失,实验测得中和热的数值偏小,故B正确; C、做本实验的室温和反应热的数据之间无关,故C错误; D、将50mL0.55mol/L氢氧化钠溶液取成了50mL0.55mol/L的氨水,由于氨水是弱碱,碱的电离是吸热的过程,所以导致实验测得中和热的数值偏小,故D正确; E、在量取盐酸时仰视计数,会使得实际量取体积高于所要量的体积,算过量,可以保证碱全反应,会使得中和和热的测定数据偏高,故E错误; F、大烧杯的盖板中间小孔太大,会导致一部分能量散失,所以测的数值降低,故F正确. 故选ABDF. |
相似问题
不能鉴别AgNO3 BaCl2 K2SO4和Mg(NO3)2四种溶液(不考虑他们之间的相互反应)的试
不能鉴别AgNO3、BaCl2、K2SO4和Mg(NO3)2四种溶液(不考虑他们之间的相互反应)的试剂是 [ ]A.盐酸、硫酸B.盐酸、氢氧化钠溶液C.氨水、硫酸D.氨水、氢氧化钠溶液
区别棉花和羊毛最简单的方法是 [ ]A.加稀硫酸后加热使之水解 检验水解产物能否与新制Cu(
区别棉花和羊毛最简单的方法是 [ ]A.加稀硫酸后加热使之水解,检验水解产物能否与新制Cu(OH)2悬浊液发生反应B.浸入浓硝酸中,观察其颜色是否变为黄色
下面有6种有机物 用提供的试剂分别鉴别 将所用试剂及产生的现象的序号填在各横线上。(1)甲苯____
下面有6种有机物,用提供的试剂分别鉴别,将所用试剂及产生的现象的序号填在各横线上。(1)甲苯____________;(2)苯乙烯____________;(3)苯酚___________
实验室用50mL0.50mol/L盐酸 50mL0.55mol/LNaOH溶液和下图所示装置进行测定
实验室用50mL0 50mol L盐酸、50mL0 55mol LNaOH溶液和下图所示装置进行测定中和热的实验,得到表中的数据:实验次数起始温度t1 ℃终止温度t2 ℃盐酸NaOH
焰色反应不呈黄色的是( )A.NaClB.Na2O2C.NaOHD.KOH
焰色反应不呈黄色的是( )A.NaClB.Na2O2C.NaOHD.KOH












