实验室用50mL0.50mol/L盐酸 50mL0.55mol/LNaOH溶液和下图所示装置进行测定
实验室用50mL0.50mol/L盐酸、50mL0.55mol/LNaOH溶液和下图所示装置进行测定中和热的实验,得到表中的数据:
(1)实验时用环形玻璃棒搅拌溶液的方法是______,不能用铜丝搅拌棒代替环形玻璃棒的理由是______. (2)经数据处理,t2-t1=3.4℃.则该实验测得的中和热△H=______[盐酸和NaOH溶液的密度按1g/cm3计算,反应后混,合溶液的比热容(c)按4.18J/(g?℃)计算]. (3)若将NaOH溶液改为相同体积、相同浓度的氨水,测得中和热为△H1,则△H1与△H的关系为:△H1______△H(填“<”、“>”或“=”),理由是______. 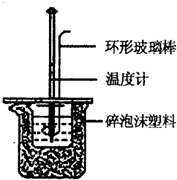 | ||||||||||||||||||
参考解答
| (1)环形玻璃搅拌棒上下搅动使溶液充分反应;不能将环形玻璃搅拌棒改为铜丝搅拌棒,因为铜丝搅拌棒是热的良导体, 故答案为:上下搅动;铜传热快,防止热量损失; (2)50mL 0.50mol?L-1盐酸、50mL 0.55mol?L-1 NaOH的质量和为m=100mL×1g/mL=100g,c=4.18J/(g?℃),t2-t1=3.4℃,代入公式Q=cm△T得生成0.025mol的水放出热量Q=4.18J/(g?℃)×100g×3.4℃=1421.2J=1.4212KJ,即生成0.025mol的水放出热量1.4212KJ,所以生成1mol的水放出热量为
故答案为:-56.8kJ/mol; (3)一水合氨为弱碱,电离过程为吸热过程,所以用氨水代替稀氢氧化钠溶液反应,反应放出的热量小于56.8kJ,所以△H1>△H, 故答案为:>;NH3?H2O电离吸热. |
相似问题
焰色反应不呈黄色的是( )A.NaClB.Na2O2C.NaOHD.KOH
焰色反应不呈黄色的是( )A.NaClB.Na2O2C.NaOHD.KOH
下列鉴别方法可行的是 [ ]A.用氨水鉴别Al3+ Mg2+和Ag+ B.用Ba(NO3)2
下列鉴别方法可行的是 [ ]A.用氨水鉴别Al3+、Mg2+和Ag+ B.用Ba(NO3)2溶液鉴别Cl-、SO42-和CO32-C.用核磁共振氢谱鉴别1-溴丙烷和2-溴丙烷D.用银氨溶液鉴别甲醛和甲酸
下叙述正确的是( )A.金属与盐溶液的反应都是置换反应B.阴离子都只有还原性C.与强酸 强碱都反应
下叙述正确的是( )A.金属与盐溶液的反应都是置换反应B.阴离子都只有还原性C.与强酸、强碱都反应的物质只有两性氧化物或两性氢氧化物D.国庆60周
某同学按照课本实验要求 用50 mL 0.50 mol/L的盐酸与50 mL 0.55 mol/L的
某同学按照课本实验要求,用50 mL 0 50 mol L的盐酸与50 mL 0 55 mol L的NaOH 溶液在下图所示的装置中进行中和反应。通过测定反应过程中所放出的
只能用焰色反应实验区分的是[ ]A.NaCl和Na2CO3B.KCl和NaClC.KCl和K
只能用焰色反应实验区分的是[ ]A.NaCl和Na2CO3B.KCl和NaClC.KCl和K2CO3 D.钠和钾












