为什么过渡元素的配合离子中八面体构型远较四面体构型多?请帮忙给出正确答案和分析 谢谢!
为什么过渡元素的配合离子中八面体构型远较四面体构型多?
请帮忙给出正确答案和分析,谢谢!
参考解答
正确答案:正八面体场及正四面体场的d1~d10的CFSE列在下表中(单位:Dq)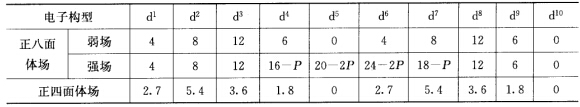 正四面体场与正八面体场的CFSE相比除d0、d10和在弱场情况下d5相等(均为0)外都是八面体场的CFSE大于四面体场的CFSE。因此在过渡元素的配合离子中正八面体远较四面体多。只有当中央离子的电子分布为d10、d10以及在弱场中的d5时才较易形成四面体配合离子。例如d0:TiCl4、ZrCl4;d10:[Zn(NH3)42+、[Cd(CN)42-、[HgI42-;d5:[FeCl4-等都是四面体配合离子。
正四面体场与正八面体场的CFSE相比除d0、d10和在弱场情况下d5相等(均为0)外都是八面体场的CFSE大于四面体场的CFSE。因此在过渡元素的配合离子中正八面体远较四面体多。只有当中央离子的电子分布为d10、d10以及在弱场中的d5时才较易形成四面体配合离子。例如d0:TiCl4、ZrCl4;d10:[Zn(NH3)42+、[Cd(CN)42-、[HgI42-;d5:[FeCl4-等都是四面体配合离子。
正八面体场及正四面体场的d1~d10的CFSE列在下表中(单位:Dq)正四面体场与正八面体场的CFSE相比,除d0、d10和在弱场情况下d5相等(均为0)外,都是八面体场的CFSE大于四面体场的CFSE。因此,在过渡元素的配合离子中,正八面体远较四面体多。只有当中央离子的电子分布为d10、d10以及在弱场中的d5时,才较易形成四面体配合离子。例如,d0:TiCl4、ZrCl4;d10:[Zn(NH3)42+、[Cd(CN)42-、[HgI42-;d5:[FeCl4-等都是四面体配合离子。
相似问题
指出下列分(离)子的杂化态及几何构型 判断所属的点群:NF3 BF3NH3 NH4+ NH2 H2S
指出下列分(离)子的杂化态及几何构型,判断所属的点群:NF3、BF3NH3、NH4+、NH2、H2S、PCl3、O3、N3、SO4-、SO3-。请帮忙给出正确答案和分析,谢谢!
已知氢的∮2s= ∮2s波函数径向分布极大值和节面处的半径是多少?概率密度极大值是多少?请帮忙给出正
已知氢的∮2s=,∮2s波函数径向分布极大值和节面处的半径是多少?概率密度极大值是多少?请帮忙给出正确答案和分析,谢谢!
A1(CH3)3的二聚分子属D2h群(与B2H6相似)。请帮忙给出正确答案和分析 谢谢!
A1(CH3)3的二聚分子属D2h群(与B2H6相似)。请帮忙给出正确答案和分析,谢谢!
求V(Z=23)原子基态时的最稳定的光谱支项。请帮忙给出正确答案和分析 谢谢!
求V(Z=23)原子基态时的最稳定的光谱支项。请帮忙给出正确答案和分析,谢谢!
求H2+中电子处于成键轨道σ1s时 它出现在键轴上离某一氢原子40pm处的两点M和N的概率密度的比值
求H2+中电子处于成键轨道σ1s时,它出现在键轴上离某一氢原子40pm处的两点M和N的概率密度的比值,已知H2+的键长为106pm,计算结果说明什么问题?请帮忙给












