下表为元素周期表的一部分 表中阿拉伯数字(1 2…)是 原周期表中行或列的序号。请参照元素A~I在表
| 下表为元素周期表的一部分,表中阿拉伯数字(1,2…)是 原周期表中行或列的序号。请参照元素A~I在表中的位置,回答下列问题: |
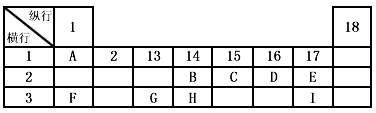 |
| (1)B、C两元素中非金属性较强的是____________(写出元素名称),请设计一个简单的实验证明这一结论:_______________。 (2)表中某元素能形成两性氧化物,写出该氧化物溶于氢氧化钠溶液的离子反应方程式______________ (3)表中某元素的单质在常温下为气态,该元素能与A~I中的一种元素构成原子个数比为1:1和1:2的两种共价化合物X和Y,该元素还能与A~I中的另一种元素构成离子个数比为1:1和1:2的两种离子化合物Z和M。写出Z与 Y反应的化学方程式:_______________。 (4)I元素在周期表里的位置是在第____周期、第____族。实验室中采用下图所示装置模拟工业上同时制取元素A 和I的单质的过程: |
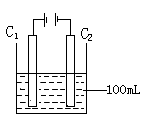 |
| ①写出电极C1上发生反应的电极反应式_____________ ②当电极上产生112 mL(标准状况)元素I单质气体时(假设气体完全逸出,溶液体积不变),烧杯中溶液的pH=___。(Kw =1.00×10-14) |
参考解答
| (1)氮 ;取碳酸钠或碳酸氢钠溶液置于试管中, 向其中滴加稀硝酸,观察是否有无色无味的气体产生,HNO3+NaHCO3=NaNO3+H2O+CO2↑ 或2 HNO3+Na2CO3=2NaNO3+H2O+CO2↑ (可不写化学方程式,其他合理的答案也可) (2)Al2O3+2OH-+3H2O=2[Al(OH)4- (3)2Na2O2+2H2O=4NaOH+O2↑ (4)三 ;ⅦA;①2Cl-→Cl2↑+2e- ;②13 |
相似问题
早在1807年化学家戴维用电解熔融氢氧化钠的方法制得钠:4NaOH(熔融)4Na+O2↑+2H2O;
早在1807年化学家戴维用电解熔融氢氧化钠的方法制得钠:4NaOH(熔融)4Na+O2↑+2H2O;后来盖—吕萨克用铁与熔融氢氧化钠作用也制得钠,反应原理为:3Fe+4Na
工业上对海水资源综合开发利用的部分工艺流程如图所示.(1)电解饱和食盐水常用离子膜电解槽和隔膜电解槽
工业上对海水资源综合开发利用的部分工艺流程如图所示.(1)电解饱和食盐水常用离子膜电解槽和隔膜电解槽.离子膜和隔膜均允许通过的分子或离子是______
以Pt为电极 电解含有金属离子M+ N3+各0.10mol的溶液 阴极析出的金属单质或气体的总物质的
以Pt为电极,电解含有金属离子M+、N3+各0 10mol的溶液,阴极析出的金属单质或气体的总物质的量(y)与导线中通过电子的物质的量(x)的关系如图所示.对
关于下列图示的说法中正确的是 [ ]A.图①表示可逆反应“CO(g) + H2O(g)CO2
关于下列图示的说法中正确的是[ ]A.图①表示可逆反应“CO(g)+H2O(g)CO2(g)+H2(g)”中的ΔH大于0 B.图②为电解硫酸铜溶液的装置,一定时间内,两电极
用a b两个质量相等的Pt电极电解AlCl3和CuSO4的混合溶液[n(AlCl3):n(CuSO
用a、b两个质量相等的Pt电极电解AlCl3和CuSO4的混合溶液[n(AlCl3):n(CuSO4)=1:9]。 t1时刻a电极得到混合气体,其中Cl2在标准状况下为224mL(忽略












