K2FeO4(高铁酸钾)在水处理 绿色高能电池制备 有机合成等方面都有广泛应用前景。K2FeO4本身
| K2FeO4(高铁酸钾)在水处理、绿色高能电池制备、有机合成等方面都有广泛应用前景。K2FeO4本身的稳定性较差,在水溶液中发生反应:4K2FeO4+10H2O=4Fe(OH)3+8KOH+3O2↑ 研究人员在保持pH约 为9.40的水溶液中对K2FeO4的稳定性研究结果如下图所示。 |
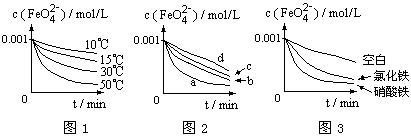 |
| 图1:K2FeO4浓度为1×10-3 mol/L 图2:K2FeO4浓度为1×10-3 mol/L,加入的另一溶质浓度为0.02 mol/L,空白指未加其它试样(a-磷酸钠 b-草酸钠 c-空白 d-醋酸钠) 图3:K2FeO4浓度为1×10-3 mol/L,加入的另一溶质浓度为5×10-4 mol/L,空白指未加其它试样。 请据此回答下列问题: (1)由图1可知,在保持pH约为9.40时,升高温度,K2FeO4的稳定性_________(填“增加”、“降低”或“不影响”)。 (2)由图2可知,在水溶液中分别加入磷酸钠、草酸钠、醋酸钠时,K2FeO4的稳定性顺序为__________________(用图中字母序号填空)。 (3)下图曲线e、f是加入NaCl的K2FeO4试样和空白对照实验所测结果。如果忽略Na+对K2FeO4稳定性的影响,其中加NaCl测得的曲线为_________。 |
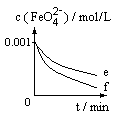 |
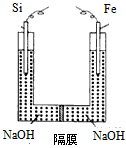
| (4)我国学者提出在浓NaOH溶液(非饱和溶液)中用电化学方法来制备高铁酸盐,电解装置如下图。电解时,阳极的电极式反应为________________________。 |
 |
| (5)K2FeO4用于处理水时,不仅能消毒杀菌,还能吸附水中的悬浮杂质。请写出K2FeO4的还原产物在水中生成Fe(OH)3的离子方程式________________________。 (6)实验室保存K2FeO4的方法是__________________________。 |
参考解答
| (1)降低 (2)d>b>a (3)f (4)Fe+8OH--6e-==FeO42-+4H2O (5)Fe3++3H2O 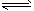 Fe(OH)3+3H+ Fe(OH)3+3H+(6)低温下密封(保持干燥)保存 |
相似问题
镍氢电池是近年开发出来的可充电电池 它可以取代会产生镉污染的镍镉电池。镍氢电池的总反应式是1/2H2
镍氢电池是近年开发出来的可充电电池,它可以取代会产生镉污染的镍镉电池。镍氢电池的总反应式是1 2H2+NiO(OH)Ni(OH)2。根据此反应式判断,下列叙述正确
用惰性电极电解下列溶液 电解一段时间后 阴极质量增加 电解液的PH下降的是[ ]A.CuSO
用惰性电极电解下列溶液,电解一段时间后,阴极质量增加,电解液的PH下降的是[ ]A.CuSO4B.AgNO3C.BaCl2D.H2SO4
如图所示 下列叙述正确的是[ ]A.Y为阴极 发生还原反应 B.X为正极 发生氧化反应 C.
如图所示,下列叙述正确的是[ ]A.Y为阴极,发生还原反应 B.X为正极,发生氧化反应 C.Y与滤纸接触处有氧气生成D.X与滤纸接触处变红
氢镍电池是近年开发出来的可充电电池 它可以取代会产生镉污染的镉镍电池。氢镍电池的总反应是根据此反应式
氢镍电池是近年开发出来的可充电电池,它可以取代会产生镉污染的镉镍电池。氢镍电池的总反应是根据此反应式判断,下列叙述中正确的是 [ ]A.电池放电时
在玻璃圆筒中盛有两种无色的互不相溶的中性液体。上层液体中插入两根石墨电极 圆筒内还放有一根下端弯成环
在玻璃圆筒中盛有两种无色的互不相溶的中性液体。上层液体中插入两根石墨电极,圆筒内还放有一根下端弯成环状的玻璃搅棒,可以上下搅动液体,装置如下图












