阅读以下信息 并回答问题.数十亿年来 地球上的物质不断地变化.大气的成分也发生了很大的变化.下表是原
| 阅读以下信息,并回答问题. 数十亿年来,地球上的物质不断地变化.大气的成分也发生了很大的变化.下表是原始大气和目前空气的主要成分:
(1)由极性键构成的非极性分子有______和______(填写化学式). (2)极易溶于水、其水溶液呈碱性的物质的分子是______(填写化学式),它之所以极易溶于水,是因为它的分子和水分子之间可形成______键. (3)分子中不含孤对电子的分子(除稀有气体外)为______(填写化学式),它的立体构型为______. (4)CO的结构可表示为  ,与CO结构最相似的分子是______(填写化学式),这两种结构相似的分子中,分子的极性______(填“相同”或“不相同”),CO分子中有一个键的形成与另外两个不同,它叫______键. ,与CO结构最相似的分子是______(填写化学式),这两种结构相似的分子中,分子的极性______(填“相同”或“不相同”),CO分子中有一个键的形成与另外两个不同,它叫______键.(5)随着原始大气中O2的缓慢增加,CH4、NH3、CO等气体逐渐被氧气氧化而缓慢地减少,使大气的成分逐渐演化成目前空气.原始大气中NH3可转化为目前空气中的______(填化学式). (6)人工模拟是当前研究的热点.有研究表明,化合物X可用于研究模拟酶,当其结合或Cu(I)(I表示化合价为+1)时,分别形成a和b: 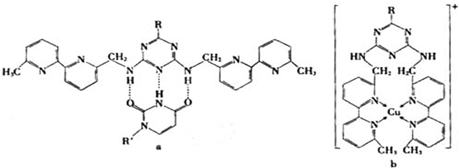 分析a和b中微粒间的相互作用(包括化学键和分子间相互作用),试指出其不同点: a中含______,b中含______.(用“氢键”、“配位键”、“极性键”、“非极性键”等填空) |
参考解答
| (1)甲烷中氮原子和氢原子之间存在极性键,甲烷是正四面体结构,正负电荷重心重合;二氧化碳分子中碳原子和氧原子之间存在极性键,二氧化碳是直线型结构,正负电荷重心重合,所以甲烷和二氧化碳是非极性分子, 故答案为:CH4;CO2; (2)氨气极易溶于水,是由于氨气能与水分子之间形成氢键,氨气溶于水,与水反应形成一水合氨:NH3+H2O?NH3?H2O?NH4++OH-,溶液呈碱性, 故答案为:NH3;氢; (3)N2、O2、CO2、水蒸气、NH3、CO的孤对电子分别为2对,4对,4对,2对,1对,2对,CH4中无孤对电子,由于碳原子采取SP3杂化,分子构型为正四面体, 故答案为:CH4;正四面体; (4)CO与N2是等电子体,等电子体的结构相似,N2是由同种元素组成的双原子分子为非极性分子;CO是由不同种元素组成的双原子分子为极性分子;由CO的结构:  可知分子含有1个配位键,2个共价键, 可知分子含有1个配位键,2个共价键,故答案为:N2;不相同;配位; (5)目前空气的主要成分N2、O2、CO2、水蒸气,由元素守恒可知原始大气中的NH3转化为现代大气中的N2和H2O,反应方程式为:4NH3+3O2=2N2+6H2O, 故答案为:N2和H2O; (6)a中碳原子和碳原子之间存在非极性键,碳原子和氮原子之间、氮原子和氢原子之间、碳原子和氢原子之间都存在极性键,氮原子和氢原子之间存在氢键;b中碳原子和碳原子之间存在非极性键,碳原子和氮原子之间、氮原子和氢原子之间、碳原子和氢原子之间都存在极性键,铜原子和氮原子间存在配位键,所以a和b中微粒间的相互作用的不同点:a中含氢键,b中含配位键, 故答案为:氢键;配位键. |
相似问题
能源问题日益成为制约国际社会经济发展的瓶颈 越来越多的国家开始实行“阳光计划” 开发太阳能资源 寻求
能源问题日益成为制约国际社会经济发展的瓶颈,越来越多的国家开始实行“阳光计划”,开发太阳能资源,寻求经济发展的新动力。(1)太阳能热水器中常使用
(8分)选择以下物质填写下列空白:A.氢氧化钠B.氧化镁 C.HeD.二氧化硅E.氯化铵
(8分)选择以下物质填写下列空白:A.氢氧化钠B.氧化镁 C.HeD.二氧化硅E.氯化铵 F.碘晶体 G.二氧化硫 H.钾(1)晶体中存在分子的是。(2)晶
某物质的实验式为PtCl4?2NH3 其水溶液不导电 加入AgNO3溶液反应也不产生沉淀 以强碱处理
某物质的实验式为PtCl4?2NH3,其水溶液不导电,加入AgNO3溶液反应也不产生沉淀,以强碱处理并没有NH3放出,则关于此化合物的说法中正确的是( )A.配
在下列有关晶体的叙述中正确的是A.晶体中有阳离子就一定存在阴离子B.分子晶体中一定存在共价键和分子间
在下列有关晶体的叙述中正确的是A.晶体中有阳离子就一定存在阴离子B.分子晶体中一定存在共价键和分子间作用力C.金属晶体的熔点一定比分子晶体高D.原
(1)向黄色的FeCl3溶液加入无色的KSCN溶液 溶液变成血红色:FeCl3+3KSCN=Fe(S
(1)向黄色的FeCl3溶液加入无色的KSCN溶液,溶液变成血红色:FeCl3+3KSCN=Fe(SCN)3+3KCl。向上述血红色溶液中加入NaF溶液振荡,只观察到血红色溶液迅速褪












