为测定混有少量氯化钠的碳酸钠(Na2CO3)固体的质量分数 向盛有12g该混合物的烧杯中加入过量稀盐
| 为测定混有少量氯化钠的碳酸钠(Na2CO3)固体的质量分数,向盛有12g该混合物的烧杯中加入过量稀盐酸,碳酸钠完全反应。反应过程用精密仪器测得烧杯和药品的质量与反应时间的数据记录如下,请根据要求回答: |
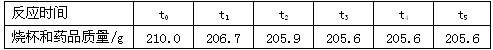 |
| (1)完全反应后,生成二氧化碳的质量是______g。 (2)请计算混合物中碳酸钠的质量分数(精确到0.1%)。 |
参考解答
| ⑴4.4g ⑵设混合物中Na2CO3的质量为x。 Na2CO3+2HCl==2NaCl+H2O+CO2↑ 106 44 x 4.4g 106:44=x:4.4g,x=10.6g 10.6g/12g×100% =88.3% 则混合物中碳酸钠的质量分数为88.3% |
相似问题
乙炔(C2H2)是一种重要的化工原料。实验室常用碳化钙(CaC2)与水反应制取乙炔 该反应的化学方程
乙炔(C2H2)是一种重要的化工原料。实验室常用碳化钙(CaC2)与水反应制取乙炔,该反应的化学方程式为:CaC2+2H2O==Ca(OH)2+C2H2↑。若要制取13g乙炔气体,
某学习小组同学用久置的过氧化氢溶液(如下图)制取氧气 取2g二氧化锰于锥形瓶中 然后慢慢滴入34g过
某学习小组同学用久置的过氧化氢溶液(如下图)制取氧气,取2g二氧化锰于锥形瓶中,然后慢慢滴入34g过氧化氢溶液,充分反应。完成下列分析及计算:⑴小明
为探究该金属粉末中Al的质量分数 取20 g该金属粉末 把100 g氢氧化钠溶液平均分成5份依次加入
为探究该金属粉末中Al的质量分数,取20 g该金属粉末,把100 g氢氧化钠溶液平均分成5份依次加入,充分反应后,过滤出固体,将其洗涤、干燥、称量。实验
用氯酸钾和二氧化锰的混合物16g 加热制取氧气。待完全反应冷却后称量 得到11.2g固体物质求:(1
用氯酸钾和二氧化锰的混合物16g,加热制取氧气。待完全反应冷却后称量,得到11 2g固体物质求:(1)生成氧气的质量是多少?(2)原混合物中二氧化锰的质
把干燥纯净的氯酸钾和二氧化锰的混合物16g装入大试管中 加热至完全反应 待试管冷却后称量 试管中剩余
把干燥纯净的氯酸钾和二氧化锰的混合物16g装入大试管中,加热至完全反应,待试管冷却后称量,试管中剩余固体质量为11 2g。求:(1)生成氧气多少克?(2












