CO2是目前大气中含量最高的一种温室气体 控制和治理CO2是解决温室效应的有效途径。(1)其中一种途
| CO2是目前大气中含量最高的一种温室气体,控制和治理CO2是解决温室效应的有效途径。 (1)其中一种途径是将CO2转化成有机物实现碳循环。如: 2CO2(g)+2H2O(l)===C2 H4(g)+3O2(g) △H=十1411.0kJ/mol 2CO2(g) +3H2 O(l)=C2 H5OH(1)十3O2(g)△H = +1366.8kJ/mol 则由乙烯水化制乙醇反应的热化学方程式为 。 (2)在一定条件下,6H2(g)+2CO2(g)  CH3CH2OH(g)+3H2O(g)。 CH3CH2OH(g)+3H2O(g)。
①温度一定时,提高氢碳比[著轰击],CO2的转化率 (填“增大”“减小” “不变”)。 ②该反应的正反应为 (填“吸”或“放”)热反应。 (3)定条件下,将3 molH2和1molCO2两种气体混合于固定容积为2L的密闭容器中,发生如下反应:3H2(g)+CO2(g) 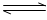 CH3OH(g)+H2O(g)。2min末该反应达到平衡,测得CH30H的浓度为0.2mol/L。下列判断不正确的是___ _。 CH3OH(g)+H2O(g)。2min末该反应达到平衡,测得CH30H的浓度为0.2mol/L。下列判断不正确的是___ _。a.该条件下此反应的化学平衡常数表达式为 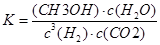 b.H2的平均反应速率为0.3mol/(L.s) c.CO2的转化率为60% d.若混合气体的密度不再改变时,该反应一定达到平衡状态 (4)如图是乙醇燃料电池(电解质溶液为KOH溶液)的结构示意图,则a处通入的是 (填“乙醇”或“氧气”),b处电极上发生的电极反应是: 。 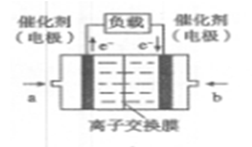 (5)CO2在自然界循环时可与CaCO3反应,CaCO3是一种难溶物质,其 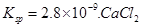 溶液与Na2CO3溶液混合可形成CaCO3沉淀,现将等体积的CaCl2溶液与Na2CO3溶液混合,若Na2CO3溶液的浓度为 溶液与Na2CO3溶液混合可形成CaCO3沉淀,现将等体积的CaCl2溶液与Na2CO3溶液混合,若Na2CO3溶液的浓度为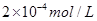 ,则生成沉淀所需CaCl2溶液的最小浓度为 。 ,则生成沉淀所需CaCl2溶液的最小浓度为 。 |
参考解答
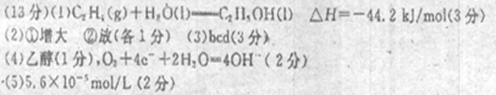 |
⑴2CO2(g)+2H2O(l)===C2 H4(g)+3O2(g) △H=十1411.0kJ/mol① 2CO2(g) +3H2 O(l)=C2 H5OH(1)十3O2(g)△H = +1366.8kJ/mol② ①-②得 C2H4(g)+H2O(l)=C2H5OH(l) △H=―44.2kJ/mol ⑵由表中看出,温度一定时,提高氢碳比[著轰击,CO2的转化率①增大;氢碳比一定,提高温度,CO2的转化率,平衡逆向移动,正确反应②放热; ⑶bcd 3H2(g)+CO2(g)  CH3OH(g)+H2O(g)。 CH3OH(g)+H2O(g)。c始 1.5 0.5 c变 0.6 0.2 0.2 0.2 c平 0.9 0.3 0.2 0.2 a.正确; b.不正确, H2的平均反应速率为0.3mol/(L.min) c.不正确,CO2的转化率为0.2/0.5×100%=40% d.不正确,混合气体的密度始终不变; ⑷a是电池的负极,原料是乙醇,O2+4e-+2H2O=4OH― ⑸2×2.8×10―9/1×10―4=5.6×10―5mol/L |
相似问题
对于达到平衡状态的可逆反应:N2+3H22NH3(正反应为放热反应)下列叙述正确的是A.反应物和生成
对于达到平衡状态的可逆反应:N2+3H22NH3(正反应为放热反应)下列叙述正确的是A.反应物和生成物的浓度相等B.N2和H2的浓度之比一定为1:3C.降低温度,平
已知重铬酸钾(K2Cr2O7)是一种比高锰酸钾还要强的氧化剂 其溶液中存在如下平衡: 2CrO42—
已知重铬酸钾(K2Cr2O7)是一种比高锰酸钾还要强的氧化剂,其溶液中存在如下平衡: 2CrO42—(黄色)+2H +Cr2O72—(橙色)+H2O若要使溶液的橙色加深,
在一定温度下 可逆反应2SO2+O22SO3达到平衡状态的标志是A.容器中SO2 O2 SO3的分子
在一定温度下,可逆反应2SO2+O22SO3达到平衡状态的标志是A.容器中SO2、O2、SO3的分子数之比为2﹕1﹕2B.单位时间内生成nmol SO3,同时消耗n 2mol O2C
CO2是目前大气中含量最高的一种温室气体 控制和治理CO2是解决温室效应的有效途径。其中一种途径是将
CO2是目前大气中含量最高的一种温室气体,控制和治理CO2是解决温室效应的有效途径。其中一种途径是将CO2转化成有机物实现碳循环。此反应达平衡时平衡常数
在溶液中 反应A+2BC分别在三种不同实验条件下进行 它们的起始状态均为c(A)=0.100 mol
在溶液中,反应A+2BC分别在三种不同实验条件下进行,它们的起始状态均为c(A)=0.100 mol·L-1、c(B)=0.200mol·L-1、c(C)=0 mol·L-1


 温度(K)
温度(K)









