(12分)已知反应:①SO3+H2O===H2SO4 ②3NO2+H2O===2HNO3+NO③2F
| (12分)已知反应:①SO3+H2O===H2SO4、②3NO2+H2O===2HNO3+NO ③2F2+2H2O===4HF+O2、④2Na+2H2O===2NaOH+H2↑、 ⑤Na2O+2HCl===2NaCl+H2O、⑥SiO2+2NaOH===Na2SiO3+H2O (1)上述反应中不属于氧化还原反应的有______________________ (填序号,下同). H2O被氧化的是______,H2O被还原的是______.属于氧化还原反应,但其中的H2O既不被氧化又不被还原的是__________________. (2) 用双线桥分析反应②:______________________________________________. (3) 用单线桥标出反应③的电子转移方向和数目_________________________. (4)写出反应④的离子方程式:______________________________________________. |
参考解答
| (12分) (1)①⑤⑥ (填序号,下同). ③、 ④、 ②. (2) 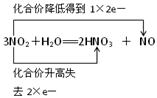  (3) (3)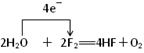 (4) 2Na+2H2O===2Na++2OH-+H2↑ |
试题分析:(1)根据方程式可知,①⑤⑥中元素的化合价都没有变化,不是氧化还原反应。而在反应②中,氮元素的化合价部分升高到+5价,部分降低到+2价,因此NO2既是氧化剂,也是还原剂,而水既不是氧化剂,也不是还原剂;反应③F元素的化合价从0价降低到-1价,单质氟是氧化剂。而水中氧元素的化合价从-2价升高到0价,失去电子,作还原剂;反应④中,钠元素的化合价从0价升高到+1价,失去电子。水中氢元素的化合价从+1价降低到0价,导电得到电子,作氧化剂。 (2)双线桥法:表示同种元素的原子在反应前后转移电子的情况,箭头从反应物指向产物,但并不表示电子转移的方向,桥两端连接同种元素,因此应该表示为 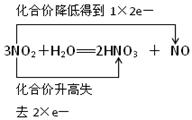 。 。(3)单线桥中箭头从还原剂中失电子的元素指向氧化剂得电子的元素,由于箭头的方向已经指明电子转移的方向,所以不需要注明得失,但必须注明电子转移的数目。即应该表示为 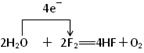 。 。(4)根据化学方程式可知,该反应的离子方程式是2Na+2H2O===2Na++2OH-+H2↑。 点评:凡是有元素化合价升降的反应都是氧化还原反应,没有元素化合价升降的反应是非氧化还原反应,所以判断氧化还原反应的关键是准确判断元素的化合价变化。 |
相似问题
下列有关氧化还原反应的说法正确的是A.浓盐酸在化学反应中既可以做氧化剂 又可以作还原剂B.工业上常以
下列有关氧化还原反应的说法正确的是A.浓盐酸在化学反应中既可以做氧化剂,又可以作还原剂B.工业上常以SiO2为原料制取粗硅,这一过程中,硅元素被氧化C
随着人们生活节奏的加快 方便的小包装食品已被广泛接受。为了防止中秋月饼等富脂食品氧化变质 延长食品的
随着人们生活节奏的加快,方便的小包装食品已被广泛接受。为了防止中秋月饼等富脂食品氧化变质,延长食品的保质期,在包装袋中常加入抗氧化物质,下列不
已知在酸性条件下能发生下列反应:Cu+→Cu+Cu2+(未配平)。NH4CuSO3与足量的2mol/
已知在酸性条件下能发生下列反应:Cu+→Cu+Cu2+(未配平)。NH4CuSO3与足量的2mol L硫酸溶液混合微热,产生下列现象:①有紫红色金属生成;②有刺激性气
(9分)现有中学化学常见的几种物质:①O2 ②Mg ③CO ④WO3 ⑤W ⑥CO2。请回答下列问题
(9分)现有中学化学常见的几种物质:①O2、②Mg、③CO、④WO3、⑤W、⑥CO2。请回答下列问题:⑴①②③④四种物质中常用作还原剂的有______________ (填序
在2KMnO4+16 HCl=2KCl+2MnCl2+5Cl2↑+8H2O的反应中 其氧化剂和还原剂
在2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O的反应中,其氧化剂和还原剂的物质的量之比为A.1∶8B.1∶5 C.8∶1 D.5∶1












