氮化铝广泛应用于电子陶瓷等工业领域。在一定条件下 AlN可通过反应:Al2O3+N2+3C2AlN+
| 氮化铝广泛应用于电子陶瓷等工业领域。在一定条件下,AlN可通过反应: Al2O3+N2+3C 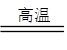 2AlN+3CO合成。下列叙述正确的是 2AlN+3CO合成。下列叙述正确的是
|
参考解答
| B |
试题分析:根据反应的化学方程式可知,氮气中氮元素的化合价从0价降低到-3价,得到3个电子。碳元素的化合价从0价升高到+2价,失去2个电子,所以氮气是氧化剂,碳是还原剂,A不正确,B正确;C不正确,AlN中氮的化合价为-3;D不正确AlN的摩尔质量为41g/mol,答案选B。 点评:该题是高考中的常见题型,属于中等难度的试题。氧化还原反应判断的关键是准确标出有关元素的化合价变化情况,然后根据有关的概念和要求逐一分析、判断即可。 |
相似问题
氰酸HCNO可消除汽车尾气中的二氧化氮 有关反应的化学方程式为:8HCNO+6NO2=7N2+8CO
氰酸HCNO可消除汽车尾气中的二氧化氮,有关反应的化学方程式为:8HCNO+6NO2=7N2+8CO2+4H2O,下列叙述中正确的是A.氮气是还原产物,二氧化碳是氧化产物B.
某校研究小组为探究KI溶液的pH与其在空气之中氧化变质的关系 进行了相应的实验探究。【提出假设】假设
某校研究小组为探究KI溶液的pH与其在空气之中氧化变质的关系,进行了相应的实验探究。【提出假设】假设1:只有碱性环境下能被氧化假设2:只有酸性环境下
如果某元素的化合价由化合态变为游离态 则它( )A.有可能被氧化 也有可能被还原B.被氧化C.
如果某元素的化合价由化合态变为游离态,则它()A.有可能被氧化,也有可能被还原B.被氧化C.由高价变为零价D.被还原
在酸性介质中 往MnSO4溶液里滴加(NH4)2S2O8溶液会发生如下离子反应:Mn2++S2O+H
在酸性介质中,往MnSO4溶液里滴加(NH4)2S2O8溶液会发生如下离子反应:Mn2++S2O+H2O→MnO+SO+H+,下列说法不正确的是()A.可以利用该反应检验Mn2+B.
已知反应:O3 + 2I- + H2O = O2 + I2 + 2OH- 下列说法不正确的是A.O3
已知反应:O3 + 2I- + H2O = O2 + I2 + 2OH-,下列说法不正确的是A.O3和O2是同素异形体B.H2O既不是氧化剂也不是还原剂C.氧化性:I2>O2D.反应生成1mol I2时转移2 mol电子












