利用食盐和氨气及二氧化碳生产纯碱的“联合制碱法”是由我国著名化学家侯德傍先生发明的.生产的关键是在沉
利用食盐和氨气及二氧化碳生产纯碱的“联合制碱法”是由我国著名化学家侯德傍先生发明的.生产的关键是在沉淀池中让原料尽可能多地转化成NaHCO3固体(因溶解度小而结晶成固体沉淀物)和主要含NH4Cl的母液,主要生产流程如下:(已知:铵盐能与碱反应产生NH3)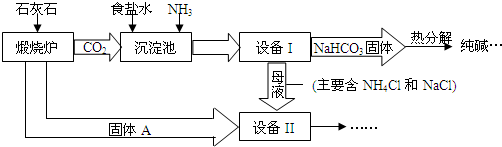 (1)“煅烧炉”中发生反应的化学方程式是______. (2)若在化学实验室里分离“设备(I)”中的混合物,用到的操作名称是______. (3)在“设备(Ⅱ)”中固体A与水反应的化学方程式是______. (4)母液在“设备(Ⅱ)”中经处理后的生成物中,除水以外可在本流程中再利用的物质有______(填写化学式). (5)NaHCO3固体热分解生成纯碱的反应方程式为:______. (6)请写出一个该生产流程的一个优点:______. |
参考解答
(1)碳酸钙在高温下分解生成二氧化碳气体和氧化钙,化学方程式为:CaCO3
(2)过滤是把不溶于液体的固体和液体分开的一种分离混合物的方法,“设备(I)”中的液体混合物中分离出析出的晶体,故可用过滤的方法; (3)氧化钙与水反应生成氢氧化钙,化学方程式为:H2O+CaO=Ca(OH)2; (4)进入“设备(Ⅱ)”的物质有氧化钙、氯化钠、氯化铵及水,发生的反应有H2O+CaO=Ca(OH)2、Ca(OH)2+2NH4Cl=2NH3↑+2H2O+CaCl2,最终产物有氯化钠、氯化钙、氨气,其中氯化钠、氨气可再利用; (5)NaHCO3固体热分解生成纯碱的反应的化学方程式为:2NaHCO3
(6)从生产过程流程图可看出,使用的原料成本低、易得,且生产流程中有些物质可循环利用原料便宜易得(或者有物质可以循环利用) 故答案为: (1)CaCO3
(2)过滤;漏斗、玻璃棒; (3)H2O+CaO=Ca(OH)2; (4)NH3、NaCl; (5)2NaHCO3
(6)原料便宜易得(或者有物质可以循环利用) |
相似问题
在一定条件下 下列物质间的转化能通过一步反应实现的是①甲烷→炭黑 ②熟石灰→烧碱 ③蛋白质→氨基酸
在一定条件下,下列物质间的转化能通过一步反应实现的是①甲烷→炭黑②熟石灰→烧碱③蛋白质→氨基酸④硫→三氧化硫⑤碳铵→氨气( )A.②⑤B.①②
下列物质间的每一转化都能通过一步反应实现的是( )A.CuO→Cu→CuOB.Na2CO3→CO2
下列物质间的每一转化都能通过一步反应实现的是( )A.CuO→Cu→CuOB.Na2CO3→CO2→Na2CO3C.O2→Fe3O4→O2D.Fe→FeCl3→Fe
A B C为初中化学常见的三种物质 他们中只含有一种相同元素 且有如图所示的反应关系(“→”表示两者
A、B、C为初中化学常见的三种物质,他们中只含有一种相同元素,且有如图所示的反应关系(“→”表示两者之间能转化) (1)若A、B、C中有一种是单质,那
有A. B. C. D. E五种常见物质 它们有如图所示的关系: 已知:C是一种金属 气体D可以使澄
有A B C D E五种常见物质,它们有如图所示的关系: 已知:C是一种金属,气体D可以使澄清石灰水变浑浊,E气体有毒,能与人体内的血红蛋白结合。
市场上有一种用于预防和治疗缺氧症状的便携式制氧器 利用过碳酸钠固体A(化学式为2Na2CO3?3H2
市场上有一种用于预防和治疗缺氧症状的便携式制氧器,利用过碳酸钠固体A(化学式为2Na2CO3?3H2O2,该物质具有碳酸钠和过氧化氢的双重性质)和灰黑色固体B












