将Cu投入足量的FeCl3的水溶液中 两者发生反应的化学方程式如下:2FeCl3+Cu═2FeCl2
| 将Cu投入足量的FeCl3的水溶液中,两者发生反应的化学方程式如下: 2FeCl3+Cu═2FeCl2+CuCl2 (1)请用双线桥法标出电子转移的方向和数目. (2)在该反应中,氧化剂是______,氧化产物是______. (3)当有0.3mol电子发生转移时,发生反应的Cu的质量为______g. (4)请将以上反应改写为离子方程式______. |
参考解答
(1)化合价升高元素是Cu,失电子,化合价降低元素是Fe,得到电子,化合价升高数=化合价降低数=转移电子数=2,双线桥法,电子转移的方向和数目如下: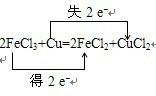 ,故答案为:  ; (2)化合价降低元素Fe元素所在的反应物FeCl3是氧化剂,对应产物FeCl2是还原产物,化合价升高元素Cu所在的反应物是还原剂,对应产物CuCl2 是氧化产物,故答案为:FeCl3;CuCl2; (3)根据方程式当有2mol电子发生转移时,发生反应的Cu的物质的量是1mol,当有0.3mol电子发生转移时,发生反应的 Cu的物质的量是0.15mol,质量是0.15mol×64g/mol=9.6g,故答案为:9.6; (4)反应2FeCl3+Cu=2FeCl2+CuCl2改为离子方程式为:2Fe3++Cu=2Fe2++Cu2+,故答案为:2Fe3++Cu=2Fe2++Cu2+. |
相似问题
下列反应中 不属于四种基本反应类型 但属于氧化还原反应的是( )A.2Na+2H2O=2NaOH+
下列反应中,不属于四种基本反应类型,但属于氧化还原反应的是( )A.2Na+2H2O=2NaOH+H2↑B.CH4+2O2点燃 CO2+2H2OC.2KClO3△ 2KCl+3O2↑D.CaCO3+2HCl=CaCl2+H2O+CO2↑
制备氰氨基化钙的化学方程式为CaCO3+2HCN=CaCN2+CO↑+H2↑+CO2↑ 在反应中(
制备氰氨基化钙的化学方程式为CaCO3+2HCN=CaCN2+CO↑+H2↑+CO2↑,在反应中( )A.氢元素被氧化,碳元素被还原B.HCN是氧化剂不是还原剂C.CaCN2是氧
2011年诺贝尔化学奖授予美日科学家 他们由于研究“有机物合成过程中钯催化交叉偶联”而获奖.钯的化合
2011年诺贝尔化学奖授予美日科学家,他们由于研究“有机物合成过程中钯催化交叉偶联”而获奖.钯的化合物氯化钯可用来检测有毒气体CO,常温下即可发生反
下列变化中 元素化合价升高的是( )A.KCl→AgClB.CuSO4→CuC.CaCO3→CO2
下列变化中,元素化合价升高的是( )A.KCl→AgClB.CuSO4→CuC.CaCO3→CO2D.H2→H2O
下列物质间反应 既属于离子反应 又属于氧化还原反应的是( )A.H2+O2B.CO+CuOC.Zn
下列物质间反应,既属于离子反应,又属于氧化还原反应的是( )A.H2+O2B.CO+CuOC.Zn+H2SO4D.NaOH+CO2












