向含1mol HCl和l mol MgSO4的混合溶液中加入1mol/L的Ba(OH)2溶液 产生沉
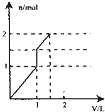
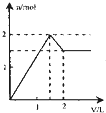
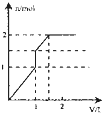
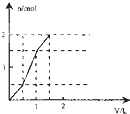
向含1mol HCl和l mol MgSO4的混合溶液中加入1mol/L的Ba(OH)2溶液,产生沉淀的物质的量(n)与加入Ba(OH)2溶液体积(V)间的关系图正确的是( )
|
参考解答
含1mol HCl和l mol MgSO4的混合溶液中加入Ba(OH)2后,首先发生反应Ba2++SO42-=BaSO4↓,生成既不溶于水又不溶于酸的BaSO4沉淀,同时OH-跟盐酸的H+发生中和反应OH-+H+=H2O,由于HCl的存在,OH-不能与Mg2+产生沉淀Mg(OH)2,待H+完全反应,OH-与Mg2+开始生成Mg(OH)2沉淀,由OH-+H+=H2O可知,H+完全反应时加入的Ba(OH)2为0.5mol,加入Ba(OH)2溶液的体积为
继续加入Ba(OH)2,发生反应Ba2++SO42-=BaSO4↓、Mg2++2OH-=Mg(OH)2↓,此时加入相同质体积的Ba(OH)2溶液,生成的沉淀的量比上一阶段要多,当再加入0.5molBa(OH)2时,溶液中的SO42-恰好沉淀,参加反应的Mg2+物质的量为0.5mol,此阶段又产生沉淀n(BaSO4)=0.5mol,n[Mg(OH)2=0.5mol,加入Ba(OH)2溶液的体积为
在继续加入Ba(OH)2溶液,发生反应Mg2++2OH-+=Mg(OH)2↓,沉淀的量继续增大,此时加入相同质体积的Ba(OH)2溶液,生成的沉淀的量较第二阶段小,但与第一阶段相同,但当再加入0.5molBa(OH)2时,0.5molMg2+完全沉淀,加入Ba(OH)2溶液的体积为
由上述分析可知三个阶段加入的加入Ba(OH)2溶液的体积相同为500mL; 第一阶段产生沉淀n(BaSO4)=0.5mol; 第二阶段又生成沉淀n(BaSO4)=0.5mol,n[Mg(OH)2=0.5mol,此时沉淀总量为1.5mol,加入Ba(OH)2溶液的总体积为1L; 第三阶段又生成沉淀n[Mg(OH)2=0.5mol,此时沉淀总量为2mol,加入Ba(OH)2溶液的总体积为1.5L. 沉淀的量与Ba(OH)2溶液体积关系图为: 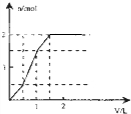 . 故选:D. |
相似问题
下列离子方程式正确的是( )A.Ca(HCO3)2溶液中加入过量NaOH溶液Ca2++HCO3-+
下列离子方程式正确的是( )A.Ca(HCO3)2溶液中加入过量NaOH溶液Ca2++HCO3-+OH-=CaCO3↓+H2OB.SO2通入溴水中SO2+Br2+2H2O═4H++2Br-+SO42-C.Cu片
下列离子方程式不正确的是( )A.向氢氧化钾溶液中滴加少量氯化铝溶液Al3++4OH-=AlO2-
下列离子方程式不正确的是( )A.向氢氧化钾溶液中滴加少量氯化铝溶液Al3++4OH-=AlO2-+2H2OB.在亚硫酸中加入过量的次氯酸钠溶液H2SO3+3ClO-=Cl-+2HC
能用Ba2++SO42-=BaSO4↓表示的是( )A.Ba(OH)2溶液和H2SO4溶液的反应B
能用Ba2++SO42-=BaSO4↓表示的是( )A.Ba(OH)2溶液和H2SO4溶液的反应B.Ba(OH)2溶液和CuSO4溶液的反应C.BaCl2溶液和H2SO4溶液的反应D.BaCl2溶液和稀NaHSO4的反应
下列离子方程式中正确的是( )A.铝与稀盐酸反应:Al+2H+═Al3++H2↑B.氯气与氢氧化钠
下列离子方程式中正确的是( )A.铝与稀盐酸反应:Al+2H+═Al3++H2↑B.氯气与氢氧化钠溶液反应:Cl2+2NaOH═H2O+Cl-+ClO-+2Na+C.钠与水反应:2Na+2
下列离子反应方程式正确的是( )A.氯气与水反应:Cl2+H2O=2H++Cl -+ClO-B.B
下列离子反应方程式正确的是( )A.氯气与水反应:Cl2+H2O=2H++Cl-+ClO-B.Ba(OH)2溶液与稀硫酸反应:Ba2++OH-+H++SO42-=BaSO4↓+H2OC.钠与水反应