陈老师在课堂上做了一个如图所示的实验 发现烧杯中酸性KMnO4溶液褪色.若将烧杯中的溶液换成含有少量
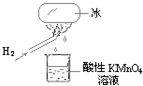
陈老师在课堂上做了一个如图所示的实验,发现烧杯中酸性KMnO4溶液褪色.若将烧杯中的溶液换成含有少量KSCN 的FeCl2溶液,溶液呈血红色.判断下列说法中正确的是( )
 |
参考解答
| 烧杯中酸性KMnO4溶液褪色,说明H2燃烧的产物中可能有还原性物质.若将烧杯中的溶液换成含有少量KSCN的FeCl2溶液,溶液呈血红色,说明有Fe3+生成,进而说明H2燃烧的产物中可能有氧化性物质,由此说明H2燃烧的产物中可能有还原性和氧化性的物质.H2O2具有氧化性与还原性,遇强氧化剂是表现还原性,遇较强的还原剂是表现氧化性. 故选:CD. |
相似问题
根据下列事实:①X+Y2+=X2++Y;②Z+H2O(冷)=Z(OH)2+H2↑;③Z2+氧化性比X
根据下列事实:①X+Y2+=X2++Y;②Z+H2O(冷)=Z(OH)2+H2↑;③Z2+氧化性比X2+弱;④由Y、W电极组成的电池,电极反应为W2++2e-=W、Y-2e-=Y2+,
下列关于氧化还原反应的叙述正确的是 [ ]A.在反应中不一定所有元素的化合价都发生变化 B
下列关于氧化还原反应的叙述正确的是 [ ]A.在反应中不一定所有元素的化合价都发生变化 B.肯定有一种元素被氧化,另一种元素被还原 C.非金属单质在
在H2O2溶液中加入KI和H2SO4的混合溶液 迅速发生反应 放出大量气体 反应过程可表示如下:①H
在H2O2溶液中加入KI和H2SO4的混合溶液,迅速发生反应,放出大量气体,反应过程可表示如下:①H2O2+2KI+H2SO4=I2+K2SO4+2H2O;②H2O2+ I2=2HIO;③H2O2+2
常温下 在下列溶液中发生如下反应: ①16H++10Z-+2XO4-=2X2+ +5Z2+8H2
常温下,在下列溶液中发生如下反应: ①16H++10Z-+2XO4-=2X2+ +5Z2+8H2O ②2A2+ +B2=2A3+ +2B- ③2B-+Z2=B2+2Z- 由此判断下列说
向CuSO4溶液中逐滴加入过量KI溶液 观察到产生白色沉淀 溶液变为棕色。再向反应后的混合物中不断通
向CuSO4溶液中逐滴加入过量KI溶液,观察到产生白色沉淀,溶液变为棕色。再向反应后的混合物中不断通入SO2气体,溶液逐渐变成无色。则下列说法正确的是[












