(1)锂电池负极材料晶体为Li+嵌入两层石墨层中导致石墨堆积方式发生改变 上下层一样 形成如图晶体结
(1)锂电池负极材料晶体为Li+嵌入两层石墨层中导致石墨堆积方式发生改变,上下层一样,形成如图晶体结构。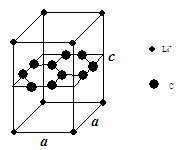 化学式为 ,该电池负极放电方程式为 。 Li+投影在石墨层图,试在图中标出与该离子邻近的其它六个Li+的投影位置。 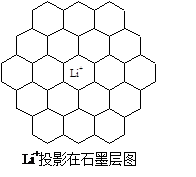 Li+与相邻石墨六元环作用力属何种键型? 。 (2)石墨中键角为 ,C原子杂化方式为 ;实验测得石墨、苯和乙烯分子中C-C键键长依次为142、140、133 pm。请对上述系列中键长依次递减的现象作出合理的解释 。 (3)第ⅡA金属碳酸盐分解温度如下:
写出BeCO3分解的化学方程式 。 分解温度为什么越来越高? 。 |
参考解答
(1) LiC6(2分) LiC6 =Li+ + 6C + e-(2分)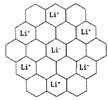 (2分) 离子键(1分) (2分) 离子键(1分)(2)120º (1分) sp2(1分) 石墨中一个C-C键平均有0.67个π电子;苯中一个C-C键平均有1个π电子;乙烯中一个C-C键平均有2个π电子;由于π电子从0.67、1增加到2,所以键长缩。(2分) (3)BeCO3 =' BeO' + CO2↑ (2分) 阳离子半径越小对氧的吸引力越大,夺取氧的能力越强。(2分) |
试题分析: (1)图中晶胞中,Li+离子在8个顶角上,平均为1个,C原子有8个在面上,平均为4,心里有2个,共6个碳原子,故化学式为LiC6,从投影来看,Li+最近的2个Li+都是沿着正六边形的一条边过去的,很容易找到其他6个投影的Li+。 (2)石墨中每个碳原子与其它3个碳原子相连,构成平面结构,故键角为120º,每个碳原子都是sp2(1分); 石墨中一个C-C键平均有0.67个π电子;苯中一个C-C键平均有1个π电子;乙烯中一个C-C键平均有2个π电子;由于π电子从0.67、1增加到2,所以键长缩。(2分) 由表中数据可知在碳酸盐中金属阴离子的半径越小,对氧原子的吸引力越大,夺取氧离子的能力越强。 |
相似问题
【化学—--选修3:物质结构与性质】(15分)金属铜与金属锰及其化合物在工业上有着广泛的应用:(1)
【化学—--选修3:物质结构与性质】(15分)金属铜与金属锰及其化合物在工业上有着广泛的应用:(1)Cu2+的外围电子排布图可表示为;(2)Mn基态原子核
下列各表中数字(表示原子序数)所表示的元素与它们在周期表中位置相符的一组是
下列各表中数字(表示原子序数)所表示的元素与它们在周期表中位置相符的一组是
已知X Y Z W四种短周期主族元素在周期表中的相对位置如图所示 其中X原子最外层电子数是其电子层数
已知X、Y、Z、W四种短周期主族元素在周期表中的相对位置如图所示,其中X原子最外层电子数是其电子层数的2倍。下列说法正确的是A.四种元素的原子半径大小
X和Y两种元素的核电荷数之和为22 X的原子核外电子数比Y的少6个。下列说法中不正确的是( )A.
X和Y两种元素的核电荷数之和为22,X的原子核外电子数比Y的少6个。下列说法中不正确的是( )A.X的单质固态时为分子晶体B.Y的单质可以形成原子晶体C.X
短周期元素X Y Z的原子序数依次增大 Y为IA族元素 X与Z同主族 三种元素原子的最外层电子数之和
短周期元素X、Y、Z的原子序数依次增大,Y为IA族元素,X与Z同主族,三种元素原子的最外层电子数之和为13。下列判断正确的是A.元素X位于第2周期第ⅣA族B.












