用二氧化氯(ClO2) 铁酸钠(Na2FeO4摩尔质量为166 g·mol-1)等新型净水剂替代传统
| 用二氧化氯(ClO2)、铁酸钠(Na2FeO4摩尔质量为166 g·mol-1)等新型净水剂替代传统的净水剂Cl2对淡水进行消毒是城市饮用水处理新技术。ClO2和Na2FeO4在水处理过程中分别被还原为Cl-和Fe3+。 (1)如果以单位质量的氧化剂所得到的电子数来表示消毒效率,那么,ClO2、Na2FeO4、Cl2三种消毒杀菌剂的消毒效率由大到小的顺序是 ▲ > ▲ > ▲ 。 (2)铁酸钠之所以能净水,除它本身具有强氧化性外,另一个原因可能是 ▲ 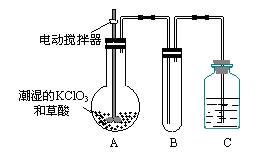 (3)二氧化氯是一种黄绿色有刺激性气味的气体,其熔点为-59℃,沸点为11.0℃,易溶于水。ClO2可以看做是亚氯酸(HClO2)和氯酸(HClO3)的混合酸酐。工业上用稍潮湿的KClO3和草酸在60℃时反应制得。某学生用如上图所示的装置模拟工业制取及收集ClO2,其中A为ClO2的发生装置,B为ClO2的凝集装置,C为尾气吸收装置。请问: ①A部分还应添加温度控制(如水浴加热)装置,B部分还应补充什么装置 ▲ ; ②该装置按①补充完整后,装置A、B、C中还有一处设计明显不合理的是 ▲ _(填“A、B或C”),理由是 ▲ ③C中应装的试剂为 ▲ 。 C中发生反应的离子方程式为: ▲ 。 |
参考解答
 |
| 略 |
相似问题
把盛有水和盐酸的两个烧杯分别放在托盘太平的左右托盘上 天平处于平衡状态 然后向右盘烧杯里加入镁 向左
把盛有水和盐酸的两个烧杯分别放在托盘太平的左右托盘上,天平处于平衡状态,然后向右盘烧杯里加入镁,向左盘烧杯里加入与镁等质量的金属钠,当金属完全
(1)(6分)卤素元素包括______ ______ ______ ______(填元素符号) 随
(1)(6分)卤素元素包括______、______、______ 、______(填元素符号),随核电荷数递增,它们的原子半径依次_______,单质的氧化性依次_______。(2
下列说法中不正确的是( )A.Cl2中的氯元素具有强氧化性 无还原性B.KI中碘元素只具有还原性
下列说法中不正确的是()A.Cl2中的氯元素具有强氧化性,无还原性B.KI中碘元素只具有还原性,而无氧化性C.Cl2与NaOH溶液反应时,既是氧化剂又是还原剂
(9分)卤素化学丰富多彩 能形成卤化物 卤素互化物 多卤化物等类型的化合物。⑴写出氯离子的离子结构示
(9分)卤素化学丰富多彩,能形成卤化物、卤素互化物、多卤化物等类型的化合物。⑴写出氯离子的离子结构示意图 ▲ 。⑵写出卤
X元素最高价氧化物对应的水化物为H3XO4 则它对应的气态氢化物为A.HXB.H2XC.XH4D.X
X元素最高价氧化物对应的水化物为H3XO4,则它对应的气态氢化物为A.HXB.H2XC.XH4D.XH3












