一定温度下 将Cl2缓慢通入水中.当通入的Cl2体积为V1时达到饱和 溶液中c(H+)变化如图中曲线
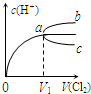
一定温度下,将Cl2缓慢通入水中.当通入的Cl2体积为V1时达到饱和,溶液中c(H+)变化如图中曲线a.已知Cl2的溶解度随温度升高而迅速降低,下列叙述中正确的是( )
 |
参考解答
| A、加水稀释促进次氯酸的电离,氢离子的物质的量增多,但体积增大,氢离子浓度反而减小,溶液中c(H+)变化如曲线c,故A错误; B、将饱和氯水升高温度,Cl2的溶解度随温度升高而迅速降低,溶液中c(H+)应减小,溶液中c(H+)变化如曲线c,故B错误; C、任何溶液都满足电中性,在饱和氯水中加入NaOH使pH>7,溶液中存在下列关系:c(Na+)+c(H+)=c(Cl-)+c(OH-)+c(ClO-),故C正确; D、溶液PH=7时,次氯酸过量,溶液中存在:c(Cl-)=c(HClO)+c(ClO-),c(Cl-)>c(ClO-),故D错误; 故选C. |
相似问题
下列处置 操作或现象的描述中正确的是( )①有大量的氯气泄漏时 应用浸有弱碱性溶液的毛巾捂住口鼻向
下列处置、操作或现象的描述中正确的是( )①有大量的氯气泄漏时,应用浸有弱碱性溶液的毛巾捂住口鼻向高处跑②用托盘天平称量50 56g KCl,0 56g通
某校化学兴趣小组用浓盐酸与二氧化锰加热反应来制取并收集氯气 装置如下:(1)写出该反应的化学方程式_
某校化学兴趣小组用浓盐酸与二氧化锰加热反应来制取并收集氯气,装置如下:(1)写出该反应的化学方程式______;反应中,氧化剂和还原剂的物质的量之比为
根据下图的转化关系完成下列有关问题。(1)写出①的离子反应方程式__________________
根据下图的转化关系完成下列有关问题。(1)写出①的离子反应方程式_________________________________。写出②的离子反应方程式_______________________
已知:①向KClO3晶体中滴加浓盐酸 产生黄绿色气体 发生反应:KClO3+6HCl=3Cl2↑+K
已知:①向KClO3晶体中滴加浓盐酸,产生黄绿色气体,发生反应:KClO3+6HCl=3Cl2↑+KCl+3H2O;②向FeCl2溶液中通入少量实验①产生的气体,溶液变黄色;③
将V(L) MgCl2溶液和V(L) NaCl溶液混合后 Cl-浓度为3 mol·L-1 则原MgC
将V(L) MgCl2溶液和V(L) NaCl溶液混合后,Cl-浓度为3 mol·L-1,则原MgCl2和NaCl两溶液物质的量浓度可能是A.都是3 mol·L-1B.分别是4 mol












