含铬化合物有毒 对人畜危害很大。因此含铬废水必须进行处理才能排放。已知:(1)在含+6价铬的废水中加
| 含铬化合物有毒,对人畜危害很大。因此含铬废水必须进行处理才能排放。 已知: 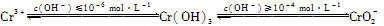 (1)在含+6价铬的废水中加入一定量的硫酸和硫酸亚铁,使+6价铬还原成+3价铬;再调节溶液pH在6~8之间,使Fe3+和Cr3+转化为Fe(OH)3、Cr(OH)3沉淀而除去。 ①写出Cr2O72-与FeSO4溶液在酸性条件下反应的离子方程式:________________。 ②用离子方程式表示溶液pH不能超过10的原因:____。 (2)将含+6价铬的废水放入电解槽内,用铁作阳极,加入适量的氯化钠进行电解。阳极区生成的Fe2+和Cr2O72-发生反应,生成的Fe3+和Cr3+在阴极区与OH-结合成氢氧化物沉淀而除去。 ①写出阴极的电极反应式:________________。 ②电解法中加入氯化钠的作用是________________。 (3)铬化学丰富多彩,由于铬光泽度好,常将铬镀在其他金属表面,同铁、镍组成各种性能的不锈钢,CrO3大量地用于电镀工业中。 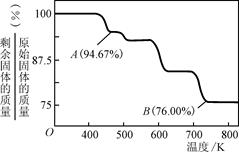 ①CrO3具有强氧化性,遇到有机物(如酒精)时,猛烈反应以至着火,若该过程中乙醇被氧化成乙酸,CrO3被还原成绿色的硫酸铬[Cr2(SO4)3]。则该反应的化学方程式为____。 ②CrO3的热稳定性较差,加热时逐步分解,其固体残留率随温度的变化如右图所示,则B点时剩余固体的成分是________________(填化学式)。 |
参考解答
| (1)①Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O ②Cr(OH)3+OH-=CrO2-+2H2O (2)①2H++2e-=H2↑(或2H2O+2e-=H2↑+2OH-) ②增强溶液导电性 (3)①4CrO3+3C2H5OH+6H2SO4=2Cr2(SO4)3+3CH3COOH+9H2O ②Cr2O3 |
试题分析::(1)二价铁离子有还原性,Cr2O72-有强氧化性,二者能发生氧化还原反应,二价铁离子被氧化成三价铁离子,Cr2O72-被还原为Cr3+,反应方程式为:Cr2O72-+6Fe2++14H+═2 Cr3++6Fe3++7H2O,故答案为:Cr2O72-+6Fe2++14H+═2Cr3++6Fe3++7H2O;②由题意可知,当pH超过10即c(OH-)≥10-4mol?L-1时,Cr(OH)3转变成CrO2-:Cr(OH)3+OH-═CrO2-+2H2O,故答案为:Cr(OH)3+OH-═CrO2-+2H2O;(2)①将含+6价铬的废水放入电解槽内,用铁作阳极,加入适量的氯化钠进行电解,阳极上铁失电子生成二价铁离子,阴极上氢离子得电子生成氢气,电极反应式为:2H++2e-═H2↑或2H2O+2e-═H2↑+2OH-,故答案为:2H++2e-═H2↑或2H2O+2e-═H2↑+2OH-;②水是弱电解质,所以蒸馏水的导电能力很小,氯化钠是强电解质,在水中能完全电离导致溶液阴阳离子浓度增大,所以能增强溶液导电性,故答案为:增强溶液导电性.(3)①CrO3具有强氧化性,遇到有机物(如酒精)时,乙醇被氧化成乙酸,碳的平均化合价从-2价升高到0,1个乙醇化合价变化4,CrO3被还原成绿色的硫酸铬[Cr2(SO4)3,铬的化合价从+6价降低到+3价,1个CrO3化合价变化3,两者的最小公倍数是12,再根据原子守恒得:4CrO3+3C2H5OH+6H2SO4=2Cr2(SO4)3+3CH3CO0H+9H2O,故答案为:4CrO3+3C2H5OH+6H2SO4=2Cr2(SO4)3+3CH3CO0H+9H2O;②设CrO3的质量为100g,则CrO3中铬元素的质量为: 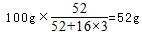 ,,B点时固体的质量为:100g×76%=76g,Co的质量没有变,所以生成物中Co的质量为52g,氧元素的质量为16,两者的个数比为 ,,B点时固体的质量为:100g×76%=76g,Co的质量没有变,所以生成物中Co的质量为52g,氧元素的质量为16,两者的个数比为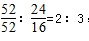 ,所以B点时剩余固体的成分是Cr2O3,故答案为:Cr2O3. ,所以B点时剩余固体的成分是Cr2O3,故答案为:Cr2O3. |
相似问题
下列离子方程式不正确的是( )A.用稀硫酸除去铜绿:4H++Cu2(OH)2CO3=2Cu2+
下列离子方程式不正确的是()A.用稀硫酸除去铜绿:4H++Cu2(OH)2CO3=2Cu2++CO2↑+3H2OB.将Na2O2固体投入H218O中:2H218O+2Na2O2=4OH-+4Na++1
下列有关离子方程式或热化学方程式书写正确的是A.石灰乳与溶液混合:B.用惰性电极电解氯化镁溶液:C.
下列有关离子方程式或热化学方程式书写正确的是A.石灰乳与溶液混合:B.用惰性电极电解氯化镁溶液:C.将碳与足量的浓硫酸共热反应后的气体混合物,通入
下列反应的离子方程式正确的是( )A.氢氧化钠溶液中通入少量二氧化硫:SO2+OH-=HSO
下列反应的离子方程式正确的是()A.氢氧化钠溶液中通入少量二氧化硫:SO2+OH-=HSO3-B.碳酸氢钠溶液与足量氢氧化钡溶液混合:HCO3-+Ba2++OH-=B
下列实验设计及其对应的离子方程式均正确的是( )A.用FeCl3溶液腐蚀铜线路板:Cu+2Fe3+
下列实验设计及其对应的离子方程式均正确的是( )A.用FeCl3溶液腐蚀铜线路板:Cu+2Fe3+=Cu2++2Fe2+B.Na2O2与H2O反应制备O2:Na2O2+H2O=2Na++
有失去标签的A B C D四瓶溶液 它们的成分可能是Na2CO3 K2SO4 Ba(NO3)2 Na
有失去标签的A、B、C、D四瓶溶液,它们的成分可能是Na2CO3、K2SO4、Ba(NO3)2、NaHSO4中的某一种,进行下列实验:(1)A+C→溶液①+气体①(2)B+A→溶液












