(10分)化学学习中有很多形如“A+B→C+D”的反应 请根据不同的情况回答下列问题:(1)如果上式
| (10分)化学学习中有很多形如“A+B→C+D”的反应,请根据不同的情况回答下列问题: (1)如果上式中A、B、C、D均为多核10电子微粒,其中A为阳离子,B为阴离子,C、D均为分子,且C的相对分子质量比D大1。则: ①A+B→C+D表示的离子方程式为 。 ②标准状况下,若2.24L的D被50mL 1mol/L硫酸吸收,则所得溶液中各离子浓度从大到小的顺序为____ 。 (2)如果上式中A、C为生活中常见的金属单质,B、D为两种氧化物且它们的摩尔质量比为12:17,其中D能与NaOH溶液反应。则: ①A+B→C+D表示的化学方程式为 。 ②D与NaOH溶液反应的化学方程式为___ 。 ③若将B溶于盐酸后,再加入足量NaOH溶液可观察到的现象为 。 |
参考解答
(1)①NH4++ OH-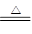 NH3↑+ H2O ②c(NH4+) > c(SO42-) > c(H+) > c(OH-) NH3↑+ H2O ②c(NH4+) > c(SO42-) > c(H+) > c(OH-)(2)① 2Al +3 FeO 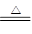 3 Fe + Al2O3 ②Al2O3 + 2NaOH ='=' 2NaAlO2 + H2O 3 Fe + Al2O3 ②Al2O3 + 2NaOH ='=' 2NaAlO2 + H2O③溶液中有白色沉淀生成,白色沉淀迅速变成灰绿色,最终变成红褐色。 |
| (1)①常见的10电子微粒是He、HF、H2O、NH3、CH4、Na+、Mg2+、Al3+、 OH-、NH4+、H3O+等。所以根据题意可知,符合条件的方程式为NH4++ OH- 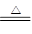 NH3↑+ NH3↑+ H2O。 ②氨气是0.1mol,硫酸是0.05mol,所以二者反应生成(NH4)2SO4,(NH4)2SO4水解显酸性,所以;离子浓度大小顺序是c(NH4+) > c(SO42-) > c(H+) > c(OH-)。 (2)①A、C为生活中常见的金属单质,B、D为两种氧化物,因此该反应应该是铝热反应,D是金属铝,B是铁。又因为B、D两种氧化物的摩尔质量比为12:17,所以B的氧化物是氧化亚铁,则方程式为 2Al +3 FeO 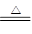 3 Fe + Al2O3。 3 Fe + Al2O3。②氧化铝是两性氧化物,和氢氧化钠溶液反应的方程式为Al2O3 + 2NaOH ='=' 2NaAlO2 + H2O。 ③铁和盐酸反应生成氯化亚铁,因此加入氢氧化钠溶液后的现象是溶液中有白色沉淀生成,白色沉淀迅速变成灰绿色,最终变成红褐色。 |
相似问题
.下列表示对应化学反应的离子方程式正确的是A.用FeCl3溶液腐蚀铜线路板:Cu + 2Fe3+=
.下列表示对应化学反应的离子方程式正确的是A.用FeCl3溶液腐蚀铜线路板:Cu + 2Fe3+= Cu2+ + 2Fe2+B.AlCl3溶液中加入过量的浓氨水:Al3++4NH3
我国有丰富的海水资源 开发和利用海水资源是当前科学研究的一项重要任务 下图是海水综合利用的一个方面。
我国有丰富的海水资源,开发和利用海水资源是当前科学研究的一项重要任务,下图是海水综合利用的一个方面。请回答下列问题:1、①步主要反应的的离子方程
下列反应的离子方程式中 书写正确的是( )A.金属钾投入到蒸馏水中:K+H2O=K++OH-+H
下列反应的离子方程式中,书写正确的是()A.金属钾投入到蒸馏水中:K+H2O=K++OH-+H2↑B.Fe跟稀盐酸反应:2Fe+6H+=2Fe3++3H2↑C.铝粉投入到NaOH
下列反应中 能用离子方程式H++OH-=H2O表示的是A.NaOH溶液和H2SiO3溶液混合B.Ba
下列反应中,能用离子方程式H++OH-=H2O表示的是A.NaOH溶液和H2SiO3溶液混合B.Ba(OH)2溶液和盐酸混合C.Al(OH)3和稀H2SO4反应D.氨水和硫酸反应
下列离子方程式正确的是:( )A.过氧化钠加入水中:2O22-+2H2O='=' 4OH-+O2↑
下列离子方程式正确的是:( )A.过氧化钠加入水中:2O22-+2H2O="=" 4OH-+O2↑B.碳酸氢钠溶液加入盐酸:CO+2H+==CO2↑+H2OC.氢氧化铜中加入盐酸:OH












