(14分)A B C D E F是原子序数依次增大的六种短周期元素。F的单质在D2中燃烧的产物可使品
| (14分)A、B、C、D、E、F是原子序数依次增大的六种短周期元素。F的单质在D2中燃烧的产物可使品红溶液褪色;B的单质在D2中燃烧可生成BD和BD2两种气体;E的原子序数为B的两倍;A元素的一种核素中不含中子。请回答下列问题: (1)C的单质分子的结构式为 ;ED的电子式为 。 (2)E单质在BD2中剧烈燃烧生成黑白两种固体,该反应的化学方程式为 。 (3)FD2气体通入BaCl2和HNO3的混合溶液中,生成白色沉淀和无色气体CD,有关反应的离子方程式为 ,由此可知CD和FD2中还原性较强的是 (填化学式)。 (4)A、C、D、F四种元素按原子个数比为5 :1 :4 :1形成化合物甲,则甲的化学式为 。将0.01mol/L的甲溶液与0.03mol/L的Ba(OH)2溶液等体积混合得到沉淀,已知该沉淀的Ksp="x" ,则混合溶液中酸根离子的浓度为 mol / L(用含x的代数式表示,混合后溶液体积变化忽略不计)。 |
参考解答
(14分)(每空2分)(1)N≡N 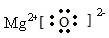 (2)2Mg+CO2 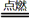 2MgO+C 2MgO+C(3)3SO2+3Ba2++2 H2O +2NO3-=3BaSO4↓+2NO↑+4 H+ SO2 (4)NH4H SO4 100x |
试题分析:A元素的一种核素中不含中子,则A是H元素;使品红溶液褪色的化合物应是SO2,所以F是S元素,D是O元素;B比D的原子序数小,且B的单质在D2中燃烧可生成BD和BD2两种气体,则B是C元素;则C是N元素,E是Mg元素。 (1)氮气分子中存在氮氮三键,所以其结构式为N≡N ;MgO是离子化合物,所以其电子式为 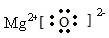 (2)E单质在BD2中剧烈燃烧生成黑白两种固体,黑色固体为单质C,白色固体为MgO,所以化学方程式为2Mg+CO2 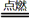 2MgO+C 2MgO+C(3)SO2气体通入BaCl2和HNO3的混合溶液中,被硝酸氧化成硫酸根离子,与钡离子结合生成硫酸钡沉淀,离子方程式为3SO2+3Ba2++2 H2O +2NO3-=3BaSO4↓+2NO↑+4 H+;在该反应中硝酸作氧化剂,NO是还原产物,SO2作还原剂,所以SO2的还原性大于NO的还原性; (4)H、N、O、S四种元素构成的化合物一般为铵盐,所以按原子个数比为5 :1 :4 :1形成化合物甲的化学式为NH4H SO4;Ba2+的物质的量是SO42-的物质的量的3倍,所以二者结合成BaSO4后,溶液中有Ba2+剩余,其物质的量浓度是(0.03mol/L-0.01mol/L)/2=0.01mol/L,根据该沉淀的Ksp=c(Ba2+)c(SO42-)='x' ,所以则混合溶液中酸根离子的浓度c(SO42-)='x/' c(Ba2+)=100x。 |
相似问题
X Y是元素周期表第ⅦA族中的两种元素。下列叙述中不能说明X的非金属性比Y强的是( )。A.X原子
X、Y是元素周期表第ⅦA族中的两种元素。下列叙述中不能说明X的非金属性比Y强的是( )。A.X原子的电子层数比Y原子的电子层数少B.酸性:HXO4>HYO4C.X的
X Y Z W均为短周期元素 它们在周期表中的位置如图所示。若X原子的最外层电子数比其次外层电子数多
X、Y、Z、W均为短周期元素,它们在周期表中的位置如图所示。若X原子的最外层电子数比其次外层电子数多3个,下列说法不正确的是A.原子半径:Z>X>YB.最高
下列有关说法正确的是A.0.1mol/LNa2CO3溶液35℃时的碱性比25℃时强 说明盐类水解反应
下列有关说法正确的是A.0.1mol LNa2CO3溶液35℃时的碱性比25℃时强,说明盐类水解反应是放热反应B.从HF、HCl、HBr、HI酸性递增的事实,推出F、Cl、Br
依据元素周期表及元素周期律 下列推断中正确的是A.同一周期元素的原子 半径越小越容易失去电子B.ⅠA
依据元素周期表及元素周期律,下列推断中正确的是A.同一周期元素的原子,半径越小越容易失去电子B.ⅠA族元素的金属性比ⅡA族元素的金属性强C.向氢硫酸
元素周期律和元素周期表是学习化学的重要工具 下列说法不正确的是( )A.同周期的主族元素中
元素周期律和元素周期表是学习化学的重要工具,下列说法不正确的是( )A.同周期的主族元素中,ⅦA族元素的原子半径最小 B.碳族元素都是非金属元素,其












