医用二水合氯化钙可用于补钙 抗过敏和消炎等 以某碳酸钙样品(其中含少量Al3+ Fe3+等杂质)生产
医用二水合氯化钙可用于补钙、抗过敏和消炎等,以某碳酸钙样品(其中含少量Al3+、Fe3+等杂质)生产医用二水合氯化钙的工艺流程为:(已知二水合氯化钙在温度超过160°C时分解为氯化钙和水)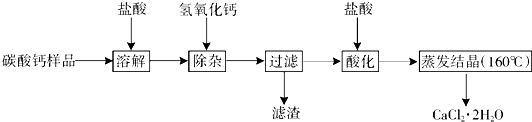 已知:查阅资料得知氢氧化物沉淀及溶解时的pH为:
(2)除杂操作是加入稍过量的氢氧化钙,调节溶液的pH使Al3+、Fe3+全部转化为沉淀,此时应该控制溶液的pH(X)范围是______;滤渣A的主要成分的化学式为______. (3)酸化时加盐酸的主要目的为了______. (4)蒸发结晶时,必须控制温度低于160℃的原因是______. (5)若所用碳酸钙样品12.5Kg,最后所得的产物中含氯化钙11.1Kg,则样品中碳酸钙的质量分数最大为多少? | ||||||||||||
参考解答
(1)在实验室进行溶解时玻璃棒的作用是加快溶解(速度),过滤时用到的玻璃仪器有烧杯、玻璃棒、漏斗. (2)根据表格中的数据,则可知加入稍过量的氢氧化钙,调节溶液的pH使Al3+、Fe3+全部转化为沉淀,此时应该控制溶液的pH(X)范围是5.2<X<7.8(或5.2-7.8);因为氢氧化钙与Al3+、Fe3+全部转化为沉淀,故滤渣A的主要成分的化学式为 Fe(OH)3、Al(OH)3. (3)利用中和反应的应用,则酸化时加盐酸的主要目的为除去过量的氢氧化钙[(Ca(OH)2或OH-. (4)“已知二水合氯化钙在温度超过160°C时分解为氯化钙和水”,则蒸发结晶时,必须控制温度低于160℃的原因是防止二水合氯化钙分解(或防止产物分解). (5)若所用碳酸钙样品12.5Kg,最后所得的产物中含氯化钙11.1Kg,则设CaCO3最大质量为x. CaCO3+2HCl═CaCl2+H2O+CO2↑ 100 111 x 11.1kg 则
答:样品中碳酸钙的质量分数最大为80%. 故答案为: (1)加快溶解(速度),漏斗 (2)5.2<X<7.8(或5.2-7.8); Fe(OH)3、Al(OH)3(少一种不给分) (3)除去过量的氢氧化钙[(Ca(OH)2或OH-; (4)防止二水合氯化钙分解(或防止产物分解) (5)80%. |
相似问题
已知常用的强酸(盐酸 硫酸 硝酸)跟常用的强碱(氢氧化钠 氢氧化钾)反应生成的盐的水溶液显中性。现将
已知常用的强酸(盐酸、硫酸、硝酸)跟常用的强碱(氢氧化钠、氢氧化钾)反应生成的盐的水溶液显中性。现将某蓝色晶体A溶入某一无色中性液体中,按下图所
甲 乙 丙是初中化学中常见的物质 其中一种物质为单质 另外两种物质组成元素相同。其转化关系如下图所示
甲、乙、丙是初中化学中常见的物质,其中一种物质为单质,另外两种物质组成元素相同。其转化关系如下图所示:(1)若甲为单质,写出相应的反应方程式。
A是常见金属单质 B C是非金属单质 且C是密度最小的气体 甲是铁在氧气中燃烧的产物 乙是无色液体
A是常见金属单质,B、C是非金属单质,且C是密度最小的气体,甲是铁在氧气中燃烧的产物,乙是无色液体,它们之间有如下的转化关系(部分产物、反应条件未标
下列物质间的转化可以实现的是( )A.Cu稀硫酸CuSO4B.CO2水H2CO3C.Fe2O3稀盐
下列物质间的转化可以实现的是( )A.Cu稀硫酸CuSO4B.CO2水H2CO3C.Fe2O3稀盐酸FeCl2D.BaCl2硫酸钾BaSO4
下列说法正确的是( )A.物质一定都有固 液 气三态B.酸一定会使石蕊试液变红 碱一定会使石蕊试液
下列说法正确的是( )A.物质一定都有固、液、气三态B.酸一定会使石蕊试液变红,碱一定会使石蕊试液变蓝C.在点燃可燃性气体前一定要检验其纯度D.












