实验室常用加热(85℃)NH4Cl和NaNO2两种饱和溶液的方法制取N2 如图是实验室用这种方法制N
| 实验室常用加热(85℃)NH4Cl和NaNO2两种饱和溶液的方法制取N2,如图是实验室用这种方法制N2,并测定生成N2体积的装置(部分装置略去),请回答相关问题: 【查阅资料】: 1、NH4Cl和NaNO2反应生成NaCl、H2O及N2,并放出大量热量; 2、20℃时,NH4Cl的溶解度约为37g; 3、N2难溶于水,实验条件下,密度为1.25g?L-1. 【实验步骤】: ①______; ②20℃时,取0.78g饱和NH4Cl溶液放入烧瓶,连接装置; ③调节水准管,使其与量气管中液面相平,记录量气管中水面读数为12mL; ④打开分液漏斗活塞,逐滴滴入饱和NaNO2溶液,加热至反应发生,移走酒精灯; ⑤烧瓶中不再产生气泡时,关闭活塞; ⑥待冷却至室温,调节两边液面高度相平,记录量气管中水面读数为VmL; ⑦处理剩余药品,整理实验台. 【实验分析及数据处理】: (1)写出装置中仪器的名称:a、______;b、______; (2)反应的化学方程式为:______; (3)完善实验步骤中的所缺部分:①______; (4)步骤④中,移走酒精灯的目的是______; (5)NH4Cl是一种______(填“易溶”、“可溶”、“微溶”、“难溶”)物质.20℃时,其饱和溶液中溶质质量分数为______.根据实验数据计算,生成氮气约为多少毫升?(计算过程中,中间数据保留2位小数,最终结果为整数;相对分子质量:Mr-NH4Cl:53.5、Mr-N2:28) (6)根据计算结果,步骤⑥中V的数值为______; (7)实验中,实际测得氮气的体积偏大,可能原因是______. A.实验中加入饱和NaNO2溶液的体积也被作为生成N2的体积 B.装置漏气. 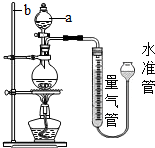 |
参考解答
| (1)熟记常见仪器的名称,a是分液漏斗,b是铁架台; (2)反应物是亚硝酸钠和氯化铵,生成物是氯化钠、水、氮气,用观察法配平,所以方程式是:NaNO2+NH4Cl═NaCl+2H2O+N2↑; (3)该反应为制取氮气的反应,所以需装置不漏气,实验前需检查装置的气密性,方法是关闭分液漏斗下端活塞并将导管连接长导管后置于水中,用酒精灯微热圆底烧瓶,若导管口有气泡冒出,撤掉酒精灯后导管内有一段水柱,则装置气密性好;反之,则装置气密性不好; (4)NaNO2+NH4Cl
(5)20℃时,NH4Cl的溶解度约为37g大于10g属于易溶物质;20℃时,其饱和溶液中溶质质量分数为:
NaNO2+NH4Cl
53.5 28 0.21g x 根据:
(6)由计算结果可知V=12mL+88mL=100mL; (7)实验中加入饱和NaNO2溶液的体积也被作为生成N2的体积,可导致实际测得氮气的体积偏大,如果装置漏气,不能测出氮气的体积. 故答案为:(1)a、分液漏斗;b、铁架台; (2)NaNO2+NH4Cl
(3)检查气密性; (4)因为反应放热,防止水准管中水冲出,影响实验(必须写出关键词“反应放热”); (5)易溶;27%;88毫升; (6)100mL; (7)A. |
相似问题
以下是一些初中常见物质相互转化的关系图(有些条件已省略)。已知:常温下甲为液体 乙和E均为黑色固体
以下是一些初中常见物质相互转化的关系图(有些条件已省略)。已知:常温下甲为液体,乙和E均为黑色固体,B是气体,D是应用最广泛的金属。请回答:(1)
现有下列物质:①纯碱 ②硫酸钾 ③水 ④生石灰 ⑤氢氧化铜 ⑥氢氧化钡 ⑦硫酸钠 ⑧硝酸钠.在实验室
现有下列物质:①纯碱、②硫酸钾、③水、④生石灰、⑤氢氧化铜、⑥氢氧化钡、⑦硫酸钠、⑧硝酸钠.在实验室里,上述物质中不能用于制烧碱的是( )A.
单质B是一种常见且用途广泛的金属 B元素在地壳中含量仅次于铝 已知金属B能发生如下一系列变化:试判断
单质B是一种常见且用途广泛的金属,B元素在地壳中含量仅次于铝,已知金属B能发生如下一系列变化:试判断:(1)写出A~E的名称:A._______;B._________
已知A B C D E是初中化学中常见的五种物质。其中A D是黑色固体 B C E是无色气体 B的相
已知A、B、C、D、E是初中化学中常见的五种物质。其中A、D是黑色固体,B、C、E是无色气体,B的相对分子质量小于C,D中含有使用最广泛的金属元素。它们在一
下图是初中化学中常见物质间的转化关系(部分反应物 生成物未列出) 其中A是一种建筑材料的主要成分 C
下图是初中化学中常见物质间的转化关系(部分反应物、生成物未列出),其中A是一种建筑材料的主要成分,C是气体,H是可用于农药的氢氧化铜。试回答下列有关












