碳酸钠用途非常广泛 是工业生产中重要的化工原料。在1921年我国科学家 侯德榜创造了一种著名的纯碱生
| 碳酸钠用途非常广泛,是工业生产中重要的化工原料。在1921年我国科学家 侯德榜创造了一种著名的纯碱生产方法--“联合制碱法”。 “联合制碱法”生产过程: (1)第一步主要反应为NH3+CO2+H2O=== NH4HCO3 该反应属于 反应(基本反应类型)。 第二步用食盐与NH4HCO3反应。食盐来源于某盐田,该粗盐主要含有氯化钠,此外还含有少量硫酸钠,氯化钙和氯化镁。经净化、精制得到生产碳酸钠所需要的食盐水,其主要流程如下: |
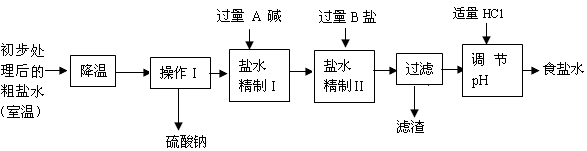 |
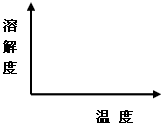
| (2)通过降温使硫酸钠从粗盐水中析出,其原理是氯化钠和硫酸钠的溶解度与温度的变化差异较大,请在溶解度图(如图)中简单画出氯化钠和硫酸钠的溶解度曲线变化趋势图。 |
 |
| (3)“精制I”操作中,加入过量含钙元素的碱的化学式是 。其反应化学方程式为 。 (4)“精制II”操作中,加入B盐的有关反应方程式为 。 (5)为保证“精制II”操作中过量B盐把杂质全部除去,请在下表中写出检验溶液中B盐是否过量的实验报告。 |
 |
| (6)查阅资料得知NaCl 、NH4HCO3、 NaHCO3 、NH4Cl在30℃时的溶解度如下表所示: |
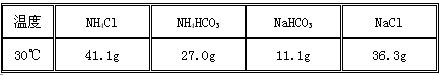 |
| 请根据溶解度表所提供的信息,写出“联合制碱法”中的第二步属于复分解反应的化学方程式: 。 第三步处理制得碳酸钠,反应原理为2NaHCO3  Na2CO3+H2O+CO2↑ Na2CO3+H2O+CO2↑ |
参考解答
| (1)化合 (2) 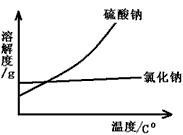 (3)Ca(OH)2 ; Ca(OH)2 + MgCl2 === Ma(OH)2↓+ CaCl2 (4)CaCl2 + Na2CO3=== 2NaCl + CaCO3↓;Ca(OH)2+Na2CO3===2NaOH + CaCO3↓ (5)方法一:  方法二:  (6)NH4HCO3+NaCl===NaHCO3↓+NH4Cl |
相似问题
为了使经济可持续发展 生产过程应尽量减少对环境的负面影响。由单质铜制取硫酸铜有下面几种步骤 其中可行
为了使经济可持续发展,生产过程应尽量减少对环境的负面影响。由单质铜制取硫酸铜有下面几种步骤,其中可行且符合以上要求的是 [ ]A Cu→CuSO4 B
金属钛(Ti)因为具有许多神奇的性能越来越引起人们的关注 被誉为“未来金属”。常温下钛不和非金属 强
金属钛(Ti)因为具有许多神奇的性能越来越引起人们的关注,被誉为“未来金属”。常温下钛不和非金属、强酸反应,加热至红热时,能与常见的非金属反应。工
下图中 “—”表示相连的物质间在一定条件下可以发生反应 “→”表示甲在一定条件下可与某种物质反应生成
下图中,“—”表示相连的物质间在一定条件下可以发生反应,“→”表示甲在一定条件下可与某种物质反应生成丙。下表四组选项中,符合下图要求的是 [ ]A
甲 乙 丙 丁四种物质在一定条件有如下转化关系(部分生成物已略去)。已知甲为红色单质 乙为黑色粉末
甲、乙、丙、丁四种物质在一定条件有如下转化关系(部分生成物已略去)。已知甲为红色单质,乙为黑色粉末,丁为白色沉淀,则图中标号①、②、③所代表的
下列各种物质间的转换通过一步反应不能实现的是 [ ]A.Fe→Fe3O4 B.CO→CO2
下列各种物质间的转换通过一步反应不能实现的是 [ ]A.Fe→Fe3O4 B.CO→CO2 C.CaCO3→CO D.CO2→H2O












