NaNO2因外观和食盐相似 又有咸味 容易使人误食中毒.已知NaNO2能发生如下反应:2NaNO2+
| NaNO2因外观和食盐相似,又有咸味,容易使人误食中毒.已知NaNO2能发生如下反应:2NaNO2+4HI═2NO↑+I2+2NaI+2H2O. (1)上述反应中氧化剂是______. (2)根据上述反应,鉴别NaNO2和NaCl.可选用的物质有:①水、②碘化钾淀粉试纸、③淀粉、④白酒、⑤食醋,你认为必须选用的物质有______(填序号). (3)某厂废液中,含有2%~5%的NaNO2,直接排放会造成污染,下列试剂能使NaNO2转化为不引起二次污染的N2的是______(填编号). A.NaClB.NH4ClC.HNO3D.浓H2SO4 (4)请配平以下化学方程式: ______Al+______NaNO3+______NaOH═______NaAlO2+______N2↑+______.若反应过程中转移5mole-,则生成标准状况下N2的体积为______L. (5)在微生物作用的条件下,NH4+经过两步反应被氧化成NO3-.两步反应的能量变化示意图如图: 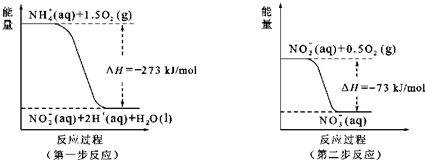 ①第一步反应是______反应(填“放热”或“吸热”),判断依据是______. ②1molNH4+(aq)全部氧化成NO3-(aq)的热化学方程式是______. |
参考解答
| (1)反应中N元素的化合价降低,I元素的化合价升高,则氧化剂是NaNO2,故答案为:NaNO2; (2)由2NaNO2+4HI═2NO↑+I2+2NaI+2H2O可知,鉴别NaNO2和NaCl,则选择②碘化钾淀粉试纸、③淀粉、⑤食醋,变蓝的为NaNO2,故答案为:②③⑤; (3)NaNO2具有氧化性,能使NaNO2转化为不引起二次污染的N2的物质应具有还原性,只有选项B符合,故答案为:B; (4)Al元素的化合价由0升高为+3价,N元素的化合价由+5价降低为0,该反应还应生成水,由电子守恒及原子守恒可知,反应为10Al+6NaNO3+4NaOH═10NaAlO2+3N2↑+2H2O,过程中转移5mole-,则生成标准状况下N2的体积为5mol×
故答案为:10;6;4;10;3;2H2O;1.12; (5)①第一步反应中,反应物总能量大于生成物总能量,则该反应为放热反应,△H<0,故答案为:放热;反应物总能量大于生成物总能量; ②1molNH4+(aq)全部氧化成NO3-(aq)可由两步反应加和得到,热化学方程式为NH4+(aq)+2O2(g)=2H+(aq)+H2O(l)+NO3-(aq)△H=-346kJ/mol, 故答案为:NH4+(aq)+2O2(g)=2H+(aq)+H2O(l)+NO3-(aq)△H=-346kJ/mol. |
相似问题
火药是我国古代的四大发明之一 成分有硫磺(S) 碳粉(C)和硝石(KNO3) 鞭炮中含有火药 点燃后
火药是我国古代的四大发明之一,成分有硫磺(S)、碳粉(C)和硝石(KNO3),鞭炮中含有火药,点燃后发生如下反应:S+2KNO3+3C=K2S+N2↑+3CO2↑,在这个
下列变化中 必须加入氧化剂的是( )A.CuO→CuSO4B.CO2→COC.H2O2→O2D.S
下列变化中,必须加入氧化剂的是( )A.CuO→CuSO4B.CO2→COC.H2O2→O2D.S2-→S
在加热时 浓硫酸与铜发生反应的化学方程式为:2H2SO4(浓)+Cu△.CuSO4+SO2↑+2H2
在加热时,浓硫酸与铜发生反应的化学方程式为:2H2SO4(浓)+Cu△ CuSO4+SO2↑+2H2O,对于该反应,下列说法中不正确的是( )A.是氧化还原反应B.铜
属于氧化还原反应的是( )A.CaCO3=CaO+CO2↑B.NH3+HCl=NH4ClC.NaO
属于氧化还原反应的是( )A.CaCO3=CaO+CO2↑B.NH3+HCl=NH4ClC.NaOH+HCl=NaCl+H2OD.Zn+H2SO4(稀)=ZnSO4+H2↑
臭氧具有强氧化性 可使湿润的碘化钾淀粉试纸变蓝 有关反应如下:O3+2KI+H2O═2KOH+I2+
臭氧具有强氧化性,可使湿润的碘化钾淀粉试纸变蓝,有关反应如下:O3+2KI+H2O═2KOH+I2+O2,对于此反应下列说法正确的是( )A.反应中O3是氧化剂,H2












